Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Сравнение кислотности и основности в разных растворителяхОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Сравнение кислотности и основности в разных растворителях Сравнение кислотности и основности в разных растворителяхСтраница 5
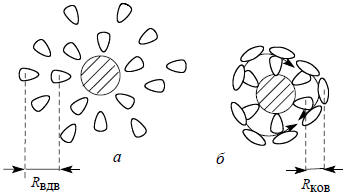
Рис. 3.5. Сольватация растворителем, состоящим из небольших (а) и больших (б) молекул
Их данных табл. 3.5 видно, что при переходе от воды (трехатомная молекула) к ДМСО (десятиатомная молекула с легко поляризуемой связью S-O) кислотность, как правило, уменьшается. Однако в случае пикриновой кислоты и 3-нитроанилина, сопряженные основания которых обладают сильной поляризуемостью (так как при ионизации возрастает степень делокализации π-электронов, поскольку (+М)-эффект группы -О- больше, а группы NH2 значительно больше мезомерного эффекта групп -ОН и -NH3+), при переходе от соды к ДМСО кислотность возрастает. Возможно, это как раз и связано с дисперсионными взаимодействиями между легко поляризуемыми анионами и легко поляризуемыми молекулами ДМСО.
Смотрите также
Анализ почв и агрохимический анализ
...
Введение.
Уравнение
Ван-дер-Ваальса используется при исследовании процессов разделения и является
базовым уравнением при качественном исследовании этих процессов.
Распространение уравнения такого типа на мно ...


