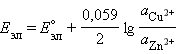Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Химические источники токаОткрытая химия / Химические источники тока / Открытая химия / Химические источники тока / Химические источники тока Химические источники токаСтраница 1
Каждый гальванический элемент состоит из двух электродов (окислительно-восстановительных пар), один из которых является поставщиком электронов (анод), а другой их принимает (катод). В гальванических элементах источником электрического тока является химическая реакция. Любая химическая реакция термодинамически разрешена, если ΔG < 0. Из соотношений ΔG = –nFE и ΔG° = –nFE° следует, что электрохимическая реакция, а в общем случае любая окислительно-восстановительная реакция может протекать самопроизвольно, если E > 0 или для стандартных условий E° > 0.
|
|
|
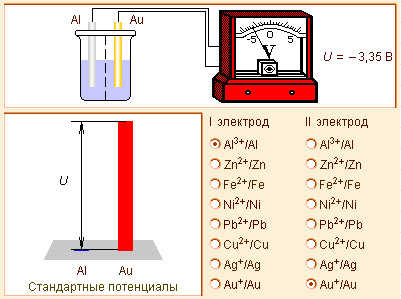
Модель 7.4. Конструктор гальванических элементов |
ЭДС гальванического элемента равна разности электродных потенциалов составляющих его электродов. В соответствии с принятой формой записи гальванического элемента его ЭДС равна электродному потенциалу правого электрода (окислителя) минус электродный потенциал левого электрода (восстановителя).
| |
| |
Пользуясь этими соотношениями и таблицей стандартных электродных потенциалов, можно предсказать возможность осуществления многих окислительно-восстановительных реакций.
В случае элемента Даниэля–Якоби (–)Zn¦Zn2+||Cu2+¦Cu(+)
| |
Для нестандартных условий ЭДС элемента Даниеля–Якоби находится из разности электродных потенциалов, вычисленных по уравнению Нернста:
| |
| |
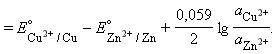 |
|
Для реакции
| |
| |
| |
Смотрите также
Равновесия в неводных растворах
...
Магнийорганические соединения
Магнийорганические
соединения относятся к числу одних из самых известных металлоорганических соединений.
Они широко применяются в органическом синтезе, хотя в последнее время их
потеснили л ...
Эволюционная химия - высшая ступень развития химических
знаний. Ближайшие перспективы химии
До недавнего
времени об эволюционной химии ничего не было известно. В отличие от биологов,
химиков не интересовал вопрос о «происхождении видов» вещества, потому что
получение любого ново ...