Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Расчет и построение диаграммы состояния Mn-Si-O при 250С. Анализ химической
устойчивостиДипломы, курсовые и прочее / Термодинамика химической устойчивости сплавов системы Mn-Si / Дипломы, курсовые и прочее / Термодинамика химической устойчивости сплавов системы Mn-Si / Расчет и построение диаграммы состояния Mn-Si-O при 250С. Анализ химической
устойчивости Расчет и построение диаграммы состояния Mn-Si-O при 250С. Анализ химической
устойчивостиСтраница 3
кремний марганец термодинамический химический равновесие
Рассчитать равновесия 10-12 не представляется возможным, что может свидетельствовать о том, что какой-либо из силицидов окисляется до силиката раньше, чем α-фаза. С этим же может быть связана и неупорядоченная последовательность вычисленных значений Р(О2).
Для того, чтобы показать термодинамическую возможность или невозможность осуществления реакций между оксидами марганца и кремния в равновесии с альфа-фазой, выполнены следующие расчёты. Для каждой из возможных реакций вычислен интервал значений Q12, удовлетворяющий условию возможности протекания этой реакции при в области составов системы Mn – Si, при которой альфа-фаза термодинамически устойчива.
1) ![]()
![]() ;
;
![]() ;
;
![]() ;
;
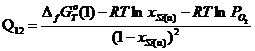 .
.
2) ![]()
![]() ;
;
![]() ;
;
![]() ;
;
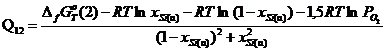 .
.
3) ![]()
![]() ;
;
![]() ;
;
![]() ;
;
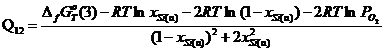 .
.
4) ![]()
![]() ;
;
![]() ;
;
![]() ;
;
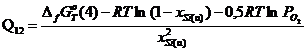 .
.
При оценке параметров Q12 необходимо учесть следующие условия: а) мольная доля кремния в альфа-фазе должна находиться в пределах существования альфа-фазы – ![]() ; б) давление кислорода в газовой фазе над конденсированной фазой не должно быть больше значения, при котором возможно окисление чистого марганца –
; б) давление кислорода в газовой фазе над конденсированной фазой не должно быть больше значения, при котором возможно окисление чистого марганца – ![]() атм. Подставляя в выражения для энергий смешения значения энергий Гиббса реакций (1) – (4), получаем следующие неравенства:
атм. Подставляя в выражения для энергий смешения значения энергий Гиббса реакций (1) – (4), получаем следующие неравенства:
Для реакции (1): ![]() ,
,
Для реакции (2): ![]() ,
,
Для реакции (3): ![]() ,
,
Для реакции (4): ![]() .
.
Сравнивая между собой полученные значения Q12, можно прийти к выводу о том, что протекание реакций между оксидами марганца и кремния в равновесии с альфа-фазой невозможно.
Таким образом, предположение о том, что окисление SiO2 до MnSiO3, MnSiO3 до Mn2SiO4, Mn2SiO4 до MnO реализуются в равновесии с альфа-фазой, не подтвердилось. Поэтому необходимо проверить предположение о том, что вышеуказанные реакции реализуются в равновесии с одним из силицидов марганца. Для этого были рассмотрены все возможные трёхфазные равновесия в системе Mn-Si-O, которые представлены в таблице.
Табл. 2.7 Все возможные трёхфазные равновесия в системе Mn-Si-O
|
Состояние |
Уравнение реакции |
|
Si – Mn11Si19 – SiO2 |
Si(A) + O2 = SiO2 |
|
Mn11Si19 – MnSi –SiO2 |
Mn11Si19 + 8O2 = 11MnSi + 8SiO2 |
|
MnSi – Mn5Si3 – SiO2 |
5MnSi + 2O2 = Mn5Si3 + 2SiO2 |
|
Mn5Si3 – Mn5Si2 – SiO2 |
Mn5Si3 + O2 = Mn5Si2 + SiO2 |
|
Mn5Si2– Mn3Si – SiO2 |
3Mn5Si2 + O2 = 5Mn3Si + SiO2 |
|
Mn3Si – Mn9Si2 – SiO2 |
3Mn3Si + O2 = Mn9Si2 + SiO2 |
|
Mn9Si2 – Mn0,85Si0,15 – SiO2 |
17Mn9Si2 + 7O2 = 180Mn0,85Si0,15 + 7SiO2 |
|
Mn0,85Si0,15 – α – SiO2 xSi(α)=0,042; aMn(α)=0,855 |
20Mn0,85Si0,15 + 3O2 = 17Mn(α) + 3SiO2 |
|
================= |
================= |
|
Mn11Si19 – SiO2 – MnSiO3 |
2Mn11Si19 + 49O2 = 22MnSiO3 + 16SiO2 |
|
MnSi – SiO2 – MnSiO3 |
2MnSi + 0SiO2 + 3O2 = 2MnSiO3 |
|
Mn5Si3 – SiO2 – MnSiO3 |
2Mn5Si3 + 4SiO2 + 11O2 = 10MnSiO3 |
|
Mn5Si2 – SiO2 – MnSiO3 |
2Mn5Si2 + 6SiO2 + 9O2 = 10MnSiO3 |
|
Mn3Si – SiO2 – MnSiO3 |
2Mn3Si + 4SiO2 + 5O2 = 6MnSiO3 |
|
Mn9Si2 – SiO2 – MnSiO3 |
2Mn9Si2 + 14SiO2 + 13O2 = 18MnSiO3 |
|
Mn0,85Si0,15 – SiO2 – MnSiO3 |
40Mn0,85Si0,15 + 28SiO2 + 23O2 = 34MnSiO3 |
|
================== |
================= |
|
Si – Mn11Si19 – MnSiO3 |
2Mn11Si19 + 33O2 = 22MnSiO3 + 16Si |
|
Mn11Si19 – MnSi – MnSiO3 |
0Mn11Si19 + 2MnSi + 3O2 = 2MnSiO3 |
|
MnSi – Mn5Si3 – MnSiO3 |
2MnSi + 3O2 = 0Mn5Si3 + 2MnSiO3 |
|
Mn5Si3 – Mn5Si2 – MnSiO3 |
6Mn5Si3 + 15O2 = 4Mn5Si2 + 10MnSiO3 |
|
Mn5Si2– Mn3Si – MnSiO3 |
4Mn5Si2 + 3O2 = 6Mn3Si + 2MnSiO3 |
|
Mn3Si – Mn9Si2 – MnSiO3 |
14Mn3Si + 9O2 = 4Mn9Si2 + 6MnSiO3 |
|
Mn9Si2 – Mn0,85Si0,15 – MnSiO3 |
4Mn9Si2 + 3O2 = 40Mn0,85Si0,15 + 2MnSiO3 |
|
Mn0,85Si0,15 – α – MnSiO3 xSi(α)=0,042; aMn(α)=0,855 |
40Mn0,85Si0,15 + 9O2 = 28Mn(α) + 6MnSiO3 |
|
================== |
================= |
|
Mn11Si19 – MnSiO3 – Mn2SiO4 |
2Mn11Si19 + 16Mn2SiO4 + 49O2 = 54MnSiO3 |
|
MnSi – MnSiO3 – Mn2SiO4 |
2MnSi + 3O2 = 0Mn2SiO4 + 2MnSiO3 |
|
Mn5Si3 – MnSiO3 – Mn2SiO4 |
2Mn5Si3 + 11O2 = 2MnSiO3 + 4Mn2SiO4 |
|
Mn5Si2 – MnSiO3 – Mn2SiO4 |
2Mn5Si2 + 2MnSiO3 + 9O2 = 6Mn2SiO4 |
|
Mn3Si – MnSiO3 – Mn2SiO4 |
2Mn3Si + 2MnSiO3 + 5O2 = 4Mn2SiO4 |
|
Mn9Si2 – MnSiO3 – Mn2SiO4 |
2Mn9Si2 + 10MnSiO3 + 13O2 = 14Mn2SiO4 |
|
Mn0,85Si0,15 – MnSiO3 – Mn2SiO4 |
40Mn0,85Si0,15 + 22MnSiO3 + 23O2 = 28Mn2SiO4 |
|
================== |
================= |
|
Si – Mn11Si19 – Mn2SiO4 |
2Mn11Si19 + 22O2 = 27Si + 11Mn2SiO4 |
|
Mn11Si19 – MnSi – Mn2SiO4 |
27MnSi + 16O2 = Mn11Si19 + 8Mn2SiO4 |
|
MnSi – Mn5Si3 – Mn2SiO4 |
Mn5Si3 + 4O2 = MnSi + 2Mn2SiO4 |
|
Mn5Si3 – Mn5Si2 – Mn2SiO4 |
Mn5Si3 + Mn5Si2 + 10O2 = 5Mn2SiO4 |
|
Mn5Si2– Mn3Si – Mn2SiO4 |
Mn5Si2 + 2O2 = Mn3Si + Mn2SiO4 |
|
Mn3Si – Mn9Si2 – Mn2SiO4 |
5Mn3Si + 6O2 = Mn9Si2 + 3Mn2SiO4 |
|
Mn9Si2 – Mn0,85Si0,15 – Mn2SiO4 |
11Mn9Si2 + 14O2 = 100Mn0,85Si0,15 + 7Mn2SiO4 |
|
Mn0,85Si0,15 – α – Mn2SiO4 xSi(α)=0,042; aMn(α)=0,855 |
20Mn0,85Si0,15 + 6O2 = 11Mn(α) + 3Mn2SiO4 |
|
================== |
================= |
|
Mn11Si19 – Mn2SiO4 – MnO |
2Mn11Si19 + 54MnO + 49O2 = 38Mn2SiO4 |
|
MnSi – Mn2SiO4 – MnO |
2MnSi + 2MnO + 3O2 = 2Mn2SiO4 |
|
Mn5Si3 – Mn2SiO4 – MnO |
2Mn5Si3 + 2MnO + 11O2 = 6Mn2SiO4 |
|
Mn5Si2 – Mn2SiO4 – MnO |
2Mn5Si2 + 9O2 = 4Mn2SiO4 + 2MnO |
|
Mn3Si – Mn2SiO4 – MnO |
2Mn3Si + 5O2 = 2Mn2SiO4 + 2MnO |
|
Mn9Si2 – Mn2SiO4 – MnO |
2Mn9Si2 + 13O2 = 4Mn2SiO4 + 10MnO |
|
Mn0,85Si0,15 – Mn2SiO4 – MnO |
40Mn0,85Si0,15 + 23O2 = 6Mn2SiO4 + 22MnO |
|
================== |
================= |
|
Si – Mn11Si19 – MnO |
2Mn11Si19 + 11O2 = 38Si(A) + 22MnO |
|
Mn11Si19 – MnSi – MnO |
19MnSi + 4O2 = Mn11Si19 + 8MnO |
|
MnSi – Mn5Si3 – MnO |
Mn5Si3 + O2 = 3MnSi + 2MnO |
|
Mn5Si3 – Mn5Si2 – MnO |
6Mn5Si2 + 5O2 = 4Mn5Si3 + 10MnO |
|
Mn5Si2– Mn3Si – MnO |
4Mn3Si + O2 = 2Mn5Si2 + 2MnO |
|
Mn3Si – Mn9Si2 – MnO |
2Mn9Si2 + 3O2 = 4Mn3Si + 6MnO |
|
Mn9Si2 – Mn0,85Si0,15 – MnO |
80Mn0,85Si0,15 + 7O2 = 6Mn9Si2 + 14MnO |
|
Mn0,85Si0,15 – α – MnO xSi(α)=0,042; aMn(α)=0,855 |
2Mn(α) + O2 = 2MnO |
|
================== |
================= |
|
MnO – Mn3O4 – Mn2SiO4 |
6MnO + O2 = 2Mn3O4 |
|
Mn3O4 – Mn2SiO4 – MnSiO3 |
6Mn2SiO4 + O2 = 6MnSiO3 + 2Mn3O4 |
|
Mn3O4 – Mn2O3 – MnSiO3 |
4Mn3O4 + O2 = 6Mn2O3 |
|
Mn2O3 – MnO2 – MnSiO3 |
2Mn2O3 + O2 = 4MnO2 |
|
MnO2 – MnSiO3 – SiO2 |
2MnSiO3 + O2 = 2MnO2 + 2SiO2 |
|
MnO2 – Mn2O7 – SiO2 |
4MnO2 + 3O2 = 2Mn2O7 |
|
Mn2O7 – SiO2 – {O2} |
Смотрите также
Тантал
В честь древнего героя
Тантала назван металл, значение которого в наши дни неизменно растет. С каждым
годом расширяется круг его применений, а вместе с этим и потребность в нем.
Однако руды его ре ...
Теоретические
основы расчета тарельчатых ректификационных колонн
Известно два
основных метода анализа работы и расчета ректификационных колонн:
графоаналитический (графический) и аналитический. Существуют некоторые
допущения, мало искажающие действительный проце ...
Выводы
Методом линейной
циклической вольтамперометрии исследовано совместное восстановление ионов
гадолиния и алюминия в хлоридных и хлоридно-фторидных расплавах на серебряном и
платиновом электродах.
...


