Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Механизмы гомогенного катализа.Статьи и работы по химии / Гомогенный катализ / Статьи и работы по химии / Гомогенный катализ / Механизмы гомогенного катализа. Механизмы гомогенного катализа.Страница 1
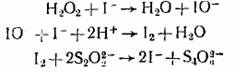 |
Эта схема представляет собой циклический маршрут с итоговым уравнением
в двух первых стадиях которого катализатор расходуется, а в последней снова регенерируется.
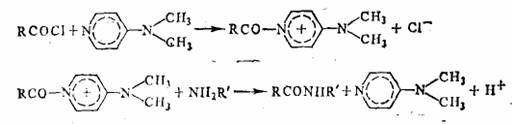
В качестве второго примера можно привести реакцию хлорангидридов карбоновых
 |
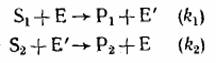 |
Такой механизм катализа часто встречается в окислительно-восстановительных реакциях, и роль катализатора в этом случае сводится к созданию нового, более эффективного пути переноса электрона от восстановителя к окислителю.
 |
Второй, наиболее распространенный механизм действия катализаторов включает в качестве первой стадии обратимое взаимодействие одного или нескольких субстратов с катализатором с образованием комплекса катализатор — субстрат. Так протекает катализ химических превращений ионами металлов и их координационными соединениями и катализ ферментами. К этому же типу можно отнести катализ кислотами, поскольку он включает, как правило, присоединение протона к одному из субстратов, что можно рассматривать как образование комплекса протон—субстрат.
Комплексообразование может приводить к нескольким различным эффектам, обеспечивающим ускорение реакции.
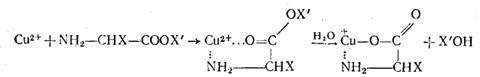 |
Смотрите также
Обсуждение результатов
Для химического
исследования снежного покрова, нами был проведен отбор проб на следующих
объектах: поселок Шлаковый, поселок Мирный, м-н. Кольное, пл. Ленина, пл.
Театральная, ЦПКиО, м-н. Канищево, ...
Химико-токсикологический анализ производных фенотиазина
В России и за рубежом, начиная
с 1945 г., после обнаружения фармакологической активности N-замещенных производных фенотиазина, было
синтезировано большое число препаратов, об ...
Синтез бис-(триметилсилил) диметиламинометил фосфоната
α-Аминофосфоновые кислоты –
структурные аналоги карбоновых α-аминокислот. Различие состоит в том, что карбоксильная
группа заменена на остаток фосфористой кислоты (PO3H2). Аминофос ...


