Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Взаимодействие серной кислоты с металлами.Статьи и работы по химии / Выполнение лабораторных работ по химии в вузах / Свойства элементов VA и VIA. / Статьи и работы по химии / Выполнение лабораторных работ по химии в вузах / Свойства элементов VA и VIA. / Взаимодействие серной кислоты с металлами. Взаимодействие серной кислоты с металлами.
Концентрированная серная кислота при нагревании окисляет почти все металлы, причем окислителем является молекула H2SO4. В зависимости от активности металла и температуры среды они восстанавливаются до SO2, S или H2S:
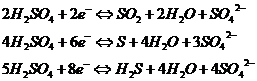
а) В пробирку поместите несколько кусочков медной стружки и налейте 1мл концентрированной серной кислоты (осторожно III). Захватив пробирку держателем, нагрейте ее нижнюю часть. Когда начнется выделение газа, осторожно определите по запаху, что за газ выделяется. Составьте уравнение реакции.
б) В пробирку поместите несколько кусочков цинка и налейте 1мл концентрированной серной кислоты (осторожно III). Захватив держателем пробирку, слегка подогрейте ее нижнюю часть и как только начнется выделение газа, определите его по запаху. Затем нагрейте пробирку и наблюдайте появление желтого осадка вследствие выделения серы. К отверстию пробирки поднесите фильтровальную бумажку, смоченную раствором соли свинца. О чем свидетельствует почернение бумажки? Составьте уравнение реакции.
Смотрите также
Производство синтетического пантотената кальция (витамина В3)
Пантотеновая кислота (витамин
В3) открыта Р. Вильямсом в 1933 г. Она была им охарактеризована как стимулятор роста дрожжей. Название свое витамин В3 получил от
греческого термина "везде ...
Введение
С давних лет человечество мечтает о лекарстве,
которое при действии на организм обладало бы максимальной избирательностью,
благодаря чему эффективно устраняется причина болезни, но не возникают
неж ...
Рабочее место руководителя
Если рассматривать рабочее место руководителя, то можно сказать, что это его рабочий кабинет, в котором он проводит большую часть работы. От того, какой это будет кабинет зависит и то, как будет работ ...


