Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
РадиоактивностьСтраница 2
Устойчивость атомного ядра зависит от отношения числа нейтронов к числу протонов, а также четности или нечетности их числа, при этом ядра с четными числами протонов и нейтронов, как правило, устойчивее ядер с нечетными числами нуклонов (табл. 11.1).
| |||||||||||||||
|
Таблица 11.1 Число устойчивых изотопов с разными числами нуклонов |
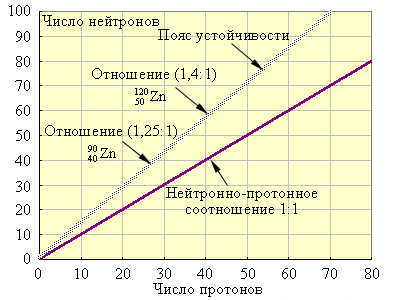
На рис. 11.1 приведен пояс устойчивости атомных ядер. Видно, что с возрастанием атомного номера отношение числа протонов к числу нейтронов для устойчивых ядер возрастает. Большинство радиоактивных изотопов расположено вне пояса устойчивости.
 |
|
Рисунок 11.1 Зависимость числа нейтронов от числа протонов в ядрах устойчивых изотопов |
Ядра с числом протонов 84 и более неустойчивы. Ядра с числом нуклонов 2, 8, 20, 28, 50, 82, 126 более устойчивы, чем ядра элементов, расположенных рядом в периодической системе. Эти числа называют магическими.
|
|
|
Модель 11.1. Стабильность ядер |
Спонтанное деление – еще один тип радиоактивного распада. Оно представляет собой самопроизвольный распад тяжелых ядер с Z ≥ 92 на два (реже на три или четыре) осколочных ядра, соответствующих середине периодической системы. Поскольку отношение N/Z для изотопов тяжелых элементов больше, чем для устойчивых изотопов середины периодической системы, спонтанное деление сопровождается испусканием 2–4 нейтронов и последующими β-распадами осколочных ядер.
Радиоактивное превращение природных радиоактивных изотопов тяжелых элементов, начинающееся с одного родоначальника и заканчивающееся стабильным изотопом, объединены в так называемые радиоактивные ряды. Теоретически возможны четыре радиоактивных ядра с массовыми числами A = 4n, 4n + 1, 4n + 2 и 4n + 3, где n – целое число. В природе обнаружены три радиоактивных ряда: ряд урана-238 (A = 4n + 2; n = 51–59), завершающийся свинцом-206, ряд тория-232 (A = 4n, n = 52–58), завершающийся свинцом-208, ряд актиноурана (A = 4n + 3, n = 51–58), начинающийся с урана-235 и завершающийся свинцом-207. Эти ряды существуют потому, что их родоначальники имеют периоды полураспада T1/2 (т. е. время, за которое распадается половина исходного количества радиоактивного изотопа), соизмеримые со временем существования Земли*). Четвертый радиоактивный ряд (A = 4n + 1, n = 52–59) называют иногда рядом нептуния (T1/2 = 2,2 млн. лет), завершается он висмутом-209.
Смотрите также
Выводы.
1.
Показано, что все исследованные способы модификации, СПИ
белковыми компонентами, позволяют п ...
Жизнь и научные открытия А.Л. Лавуазье и К.Л. Бертолле
Лавуазье и Бертолле – без сомнения, самые выдающиеся
ученые-химики своего времени. И по праву считаются основателями современной
химии, создателями принятой ныне химической номенклатуры.
...