Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Нуклеофильное замещение галогена в молекуле органического
соединения. Основные сведения о механизме реакцииДипломы, курсовые и прочее / Технология нуклеофильного замещения функциональных групп в органических соединениях / Дипломы, курсовые и прочее / Технология нуклеофильного замещения функциональных групп в органических соединениях / Нуклеофильное замещение галогена в молекуле органического
соединения. Основные сведения о механизме реакции Нуклеофильное замещение галогена в молекуле органического
соединения. Основные сведения о механизме реакцииСтраница 1
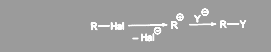
Нуклеофильное замещение в ряду галогеналканов может осуществляться как по SN1, так и по SN2 механизмам. В первом случае лимитирующей скорость процесса стадией является диссоциация галогеналкана по связи С - Hal с образованием карбкатиона:
 (1)
(1)
Таким образом, скорость процесса в этом случае не должна зависеть от концентрации нуклеофила. При достаточно большом времени существования иона карбения для оптически активных галогеналканов должна наблюдаться рацемизация. При соизмеримых величинах констант скоростей последовательных стадий процесса одна сторона катиона будет экранирована сольватированным галогенид-анионом и атака нуклеофила будет более вероятна с другой стороны, что приведет к преимущественному обращению конфигурации. Однако основной причиной отсутствия полной рацемизации является то, что во многих случаях продукты реакции образуются не из свободных карбкатионов, а из ионных пар.
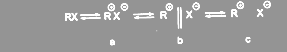 (2)
(2)
Молекула исходного соединения может диссоциировать с образованием контактной ионной пары (а), сольватно – разделённой ионной пары (b) и диссоциированных сольватирорванных ионов (с). В контактной ионной паре ассиметрия в значительной мере сохраняется, а потому нуклеофильная атака приводит к обращению конфигурации. При атаке сольватно – разделённой ионной пары селективность снижается, что приводит к общей рецемизации. Если образуется свободный радикал, то рецемизация должна быть полной. Обычно обращение конфигурации при механизме SN1 составляет от 5 до 20%.
В случае молекулярного замещения может протекать ряд побочных процессов, протекающих через стадию образования иона карбения, в частности элиминирование (Е1):
![]() (3)
(3)
Бимолекулярное замещение SN2 обычно происходит как синхронный процесс:
![]() (4)
(4)
При этом механизме нуклеофил Y приближается к субстрату со стороны, противоположной проходящей группе. Реакция представляет собой одностадийный процесс, в котором промежуточное соединение не образуется. Связь С-Y образуется одновременно с разрывом связи С-Х. В переходном состоянии исходная sp3-гибридизацию с примерно перпендикулярной р-орбиталью. Одна доля этой р-орбитали перекрывается с нуклеофилом, а вторая с уходящей группой. Поэтому механизм SN2, В котором происходила бы фронтальная атака, иногда не наблюдается.
При таком механизме скорость процесса существенно зависит как от природы, так и от концентрации нуклеофила. Реакция всегда сопровождается обращением конфигурации. Побочной может быть реакция Е2. [2]
Необходимо помнить о том, что термины SN1 и SN2 указвают лишь на молекулярность, но не на порядок реакции. Поэтому скорость реакции, протекающей по механизму SN2, будет отвечать уравнению второго порядка лишь в случае, когда оба компонента находятся в малых контролируемых концентрациях. При большом избытке нуклеофильного агента реакция может протекать по первому или дробному. Аналогичное положение может создаться, когда оба компонента не являются кинетически независимыми (например, при образовании ионных пар при неполярных растворителях). Ингольд отмечает, что и для реакции SN1 не всегда характерен первый порядок.
Очевидно, что влияние полярности среды на скорость и механизм процесса будет достаточно сильным.
Тип механизма (SN1 или SN2) зависит от структуры реагирующих соединений. Природа галогена обычно мало влияет на механизм реакции, но значительно изменяет ее скорость. С увеличением разветвленности R начинает преобладать механизм SN1, так как при этом создаются стерические препятствия для прохождения реакции по механизму SN2 и увеличивается стабильность промежуточного карбкатиона. Чем выше нуклеофильность реагента, тем вероятнее механизм SN2. [1]
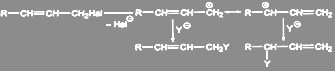
Аллилгалогениды легко вступают в реакции нуклеофильного замещения. В условиях, благоприятных для протекания мономолекулярных реакций, образуется смесь двух соединений, так как промежуточный мезомерный аллилкатион может в зависимости от условий приводить к двум разным продуктам:
 (5)
(5)
При механизме SN2 перегруппировка не происходит:
 (6)
(6)
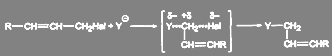
Если подход сильного нуклеофила к атому углерода при галогене стерически затруднен, то в неполярном растворителе реакция может идти с аллильной перегруппировкой при сохранении механизма SN2:
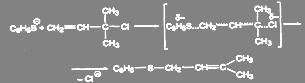 (7)
(7)
Смотрите также
Методика проведения потенциометрического титрования.
Рассмотрим процесс
потенциометрического титрования сильной кислоты раствором сильной щелочи. ...


