Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Образование общей электронной пары.Статьи и работы по химии / Атомно-молекулярное учение и его законы / Химическая связь и строение молекул. / Статьи и работы по химии / Атомно-молекулярное учение и его законы / Химическая связь и строение молекул. / Образование общей электронной пары. Образование общей электронной пары.Страница 3
N O F
Увеличение числа неспаренных электронов у атомов этих элементов возможно лишь в результате перехода одного из электронов в следующий, M-слой. Затраты энергии, требующиеся для такого перехода, очень велики. Они не компенсируются энергией, выделяющейся при образовании ковалентных связей. Поэтому у атомов названных элементов увеличение числа неспаренных электронов не наблюдается, и за счёт имеющихся в атоме неспаренных электронов атом азота образует три ковалентные связи, атом кислорода ¾ две, а атом фтора ¾ лишь одну связь. Азот, имеющий три неспаренных 2p-электрона, в соединениях с водородом или металлами трехвалентен; кислород, имеющий два неспаренных электрона, двухвалентен, а фтор при взаимодействии с водородом или металлами ведет себя как одновалентный элемент.
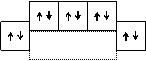
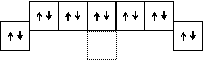
Образование молекул азота и фтора можно представить следующей схемой:
2p 2p
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 2s 2s
2s 2s
N F
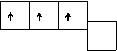 | 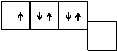 |
![]()
![]()
![]()
![]() 2p N 2p F
2p N 2p F
2s 2s
8 электронов 8 электронов
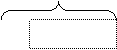 | 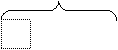 |
 |  | ||||
8 электронов 8 электронов
N2 F2
В атомах элементов III периода электроны расположены в трёх слоях, причём внешний слой, характеризующийся главным квантовым числом три, содержит электроны лишь на орбиталях 3s и 3p, в то время как M-орбиталь остаётся вакантной. Например, в атомах серы и хлора в невозбуждённом состоянии электроны располагаются следующим образом:
Смотрите также
Реакции спиртов. Кислотно-основные свойства спиртов. Реакции с участием нуклеофильного центра
Спирты представляют собой соединения
общей формулы ROH, в которых гидроксильная группа присоединена к насыщенному
атому углерода. По номенклатуре ИЮПАК насыщенные спирты называют алканолами, ...
Физико-химические основы адсорбционной очистки воды от органических веществ
Объем потребляемой в мире воды достигает 4 трлн. м3 в год, а
преобразованию со стороны человека подвергается практически вся гидросфера.
Химическая и нефтехимическая отрасли промышленности с ...
Пирит
Пирит - минерал,
дисульфид железа FeS2, самый распространенный в земной коре сульфид.
Другие названия минерала и его разновидностей: кошачье золото, золото дурака,
железный колчедан, марказит, брав ...


