Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Результаты исследованияДипломы, курсовые и прочее / Роль свободных радикалов в природной среде / Дипломы, курсовые и прочее / Роль свободных радикалов в природной среде / Результаты исследования Результаты исследованияСтраница 1
В ходе проводившихся экспериментов установлено, что в любой отдельно взятой пробе природной воды наблюдается естественное увеличение водородного показателя во времени. Эта тенденция проявляется независимо от того, была ли проба оставлена на свету или в темноте. В случае предварительного кипячения пробы в течение 20 минут значительное возрастание рН начинается примерно через три недели после начала эксперимента, а если при этом дополнительно вводился обеззараживающий агент (перекись водорода в количестве 500 мг/л), то после начального подъема рН оставался стабильным в течение всего времени наблюдений (см. рис. 2.1). Уменьшение рН на кривой 2 в первые дни проведения опыта объясняется постепенным растворением углекислоты, удаленной в результате кипячения, а начальное увеличение рН на кривой 3 будет подробнее рассмотрено ниже.
Величина подщелачивания практически не зависит от седиментации дисперсных частиц — повышение рН происходило равномерно по высоте сосуда, незначительные отклонения наблюдались лишь у самого дна. Параллельно подщелачиванию в опытах без добавления ![]() зафиксировано также некоторое возрастание оптической плотности раствора (1-2%). Возможное объяснение: возрастание доли ионизированных органических молекул. После стабилизации рН появлялась тенденция к снижению оптической плотности раствора, возможно вследствие окисления двойных связей растворенных фульвокислот. Во время проведения каждого опыта с речной водой выпадал бурый осадок гуминовых соединений, даже в случае предварительного фильтрования пробы через плотную фильтровальную бумагу для тонкодисперсных примесей.
зафиксировано также некоторое возрастание оптической плотности раствора (1-2%). Возможное объяснение: возрастание доли ионизированных органических молекул. После стабилизации рН появлялась тенденция к снижению оптической плотности раствора, возможно вследствие окисления двойных связей растворенных фульвокислот. Во время проведения каждого опыта с речной водой выпадал бурый осадок гуминовых соединений, даже в случае предварительного фильтрования пробы через плотную фильтровальную бумагу для тонкодисперсных примесей.
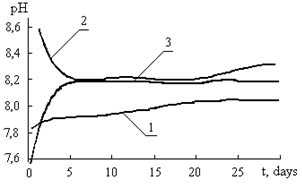
Рис. 2.1. Изменение рН в пробах речной воды: 1 — речная вода без воздействий, 2 — кипяченая речная вода, 3 — кипяченая речная вода с добавлением ![]()
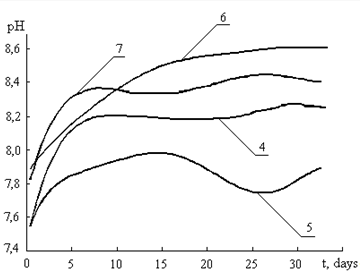
Рис. 2.2. Влияние добавок ![]() на изменение рН в водных системах: 4 — речная вода на свету, 5 — речная вода в темноте, 6 — модельный раствор без добавления
на изменение рН в водных системах: 4 — речная вода на свету, 5 — речная вода в темноте, 6 — модельный раствор без добавления ![]() , 7 — модельный раствор с добавлением
, 7 — модельный раствор с добавлением ![]()
На повышение рН оказывает некоторое влияние выщелачивание стеклянной посуды, но контрольные опыты с дистиллированной кипяченой водой в закрытом сосуде показали, что изменение рН в этом случае начинает фиксироваться ионометром лишь через 20-25 дней после начала опыта и по абсолютной величине соответствует изменению концентрации ионов водорода ![]() моль/л. За такой же период времени концентрация ионов водорода изменилась в пробе речной воды примерно на
моль/л. За такой же период времени концентрация ионов водорода изменилась в пробе речной воды примерно на ![]() моль/л, а в ряде случаев в системах с добавлением перекиси водорода произошли изменения порядка
моль/л, а в ряде случаев в системах с добавлением перекиси водорода произошли изменения порядка ![]() моль/л.
моль/л.
В случае добавления перекиси водорода эффект возрастания рН проявлялся значительно быстрее, причем отмечено увеличение рН после добавления перекиси водорода в пробы со стабилизировавшимся водородным показателем. В качестве обеззараживающей добавки перекись водорода выбрана не случайно. Этот окислитель в незначительных количествах постоянно присутствует в речной воде и активно участвует в процессах самоочищения. Существует несколько путей поступления ![]() в природные воды. Перекись водорода является одним из промежуточных продуктов метаболизма водных микроводорослей. Фотохимические реакции получения
в природные воды. Перекись водорода является одним из промежуточных продуктов метаболизма водных микроводорослей. Фотохимические реакции получения ![]() и гидроксильных радикалов будут рассмотрены ниже. В ходе опытов вводились высокие концентрации
и гидроксильных радикалов будут рассмотрены ниже. В ходе опытов вводились высокие концентрации ![]() — порядка 500 мг/л — в связи с тем, что перекись водорода активно участвовала в реакциях окисления водной органики (расход составлял примерно 23-28% за неделю наблюдений), а стерильность раствора необходимо было обеспечить в течение всего опыта.
— порядка 500 мг/л — в связи с тем, что перекись водорода активно участвовала в реакциях окисления водной органики (расход составлял примерно 23-28% за неделю наблюдений), а стерильность раствора необходимо было обеспечить в течение всего опыта.
Смотрите также
Химико-токсикологический анализ лекарственных средств, производных фенотиазина
В России и за рубежом, начиная с 1945 г., после обнаружения фармакологической активности N-замещенных производных фенотиазина, было синтезировано большое число
препаратов, обладающих нейролеп ...
Электролиз.
Цель работы - ознакомление
с процессами, протекающими на растворимых и нерастворимых электродах при
электролизе водных растворов электролитов.
Электролиз - это
окислительно-восстановительный ...
Основы метода потенциометрического
титрования.
Рассмотрим основные
понятия потенциометрического титрования, его виды и методы проведения, способы установления
точки эквивалентности при титровании. ...


