Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Растворы неэлектролитовОткрытая химия / Растворы / Открытая химия / Растворы / Растворы неэлектролитов Растворы неэлектролитов
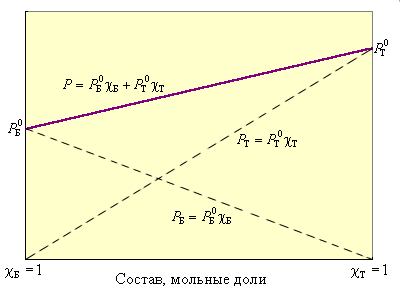
По термодинамическому признаку растворы делятся на идеальные и реальные. Для идеальных растворов предполагается, что между компонентами раствора любыми взаимодействиями можно пренебречь. Следовательно, любое свойство растворяемых веществ при их смешении не должно меняться. Например, при смешении близких по свойствам бензола и толуола давление пара P над раствором в соответствии с законом Рауля будет аддитивной величиной
|
Здесь и
,
и
– соответственно давление и мольные доли бензола и толуола.
 |
|
Рисунок 6.1 Зависимость давления пара над смесью бензол–толуол от мольной доли |
Если раствор сохраняет свойства идеальности при любых концентрациях, его называют идеальным (растворы изотопов). Часто раствор приобретает эти качества только при достаточно большом разведении, это – «бесконечно разбавленный» раствор при χ → 0. Во всех прочих случаях раствор считается реальным.
Взаимодействие между компонентами раствора, выражаемое через энтальпию сольвации ΔHсольв, служит в определенных пределах мерой идеальности раствора. Д. И. Менделеев показал, что взаимодействие между компонентами раствора может рассматриваться как химический процесс образования соединений переменного состава – сольватов. Этот подход лежит в основе химической или сольватной теории растворов. Если при кристаллизации твердая фаза содержит молекулы растворителя, то ее называют кристаллосольватом.
Смотрите также
Исследование некоторых физико-химических свойств протеиназы Penicillium wortmannii
...
Экспериментальные
результаты и обсуждения
Зависимости
поверхностного давления от площади, приходящейся на одну молекулу (p-A изотермы) для
гомо - и гетеромолекулярных плавающих слоев на основе С60, ДБ24К8 и магнитного
комплекс пр ...
Основания
Химия сегодня прочно
вошла в нашу жизнь вместе с новыми материалами, продуктами, лекарствами, синтетическими
волокнами, пластиками. В мире появляется все больше информации о новых веществах
...


