Пример 5.1) Реакция разложения дийодэтана C2H4J2 = C2H4+J2 описывается единым уравнением Аррениуса и в газовой фазе, и в растворе в CCl4. Этот случай наиболее прямое свидетельство в пользу единой кинетической модели реакции в газе и в жидкости. Распределение Максвелла-Больцмана оказывается в растворе ещё устойчивее, чем в газе, и теория активных соударений оказывается весьма удачной. Причина этого состоит в особенно эффективном механизме перераспределения энергии при соударениях частиц в жидкой фазе. График температурной зависимости константы скорости этой реакции качественно выглядит примерно следующим образом.
|
Следует далее обязательно рассмо
треть кинетические модели элементарных процессов, показывая общность кинетических приёмов описания процессов. Это:
-кинетические модели случайных дви-жений, -внутримолекулярные движения, -эмиссия и абсорбция фотонов, -время жизни, время корреляции и константа скорости, -средние хронологические физические наблюдаемые в случайных движениях .
| |
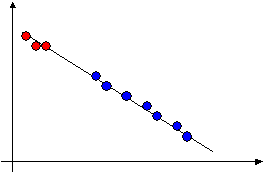
Рис. 9. Пример единой аррениусовской зависимости в газовой и жидкой фазах.



