Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Формальная кинетика сложных реакцийУчим химию / Учим химию / Формальная кинетика сложных реакций Формальная кинетика сложных реакцийСтраница 2
б) Если значительно превалирует константа скорости 2-й стадии, то промежуточный продукт находится в системе в минимальных количествах, 1-я стадия лимитирующая и определяет вид кинетической кривой накопления продукта B. Вторая стадия на графике как бы не просматривается.
в) Может иметь место случай сравнимых скоростей обеих стадий реакции. Это случай и более сложный, и менее однозначный. Эти положения достаточно легко иллюстрируются графически (см. учебник Краснова).
Двусторонние (обратимые) реакции первого порядка
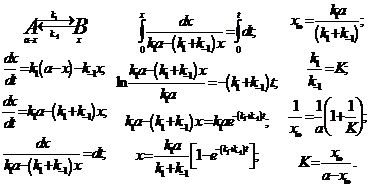
Проблема систематического описания сложных реакций сложна, и в наиболее общем виде решается лишь численными (и не аналитическими) методами . Разработаны различные аналоговые методы, позволяющие даже в очень непростых случаях эффективно графически моделировать кинетические кривые. Вместе с тем часто есть возможность избежать последовательного решения системы дифференциальных уравнений, заменяя точные решения приближёнными. Не располагая возможностью рассмотреть всю проблему в полном объёме, мы вынуждены ограничиться лишь несколькими характерными примерами …
1) Метод квазистационарных концентраций Боденштейна
Рассмотрим примеры сложных реакций, представляющих собою суперпозицию последовательных и параллельных превращений и введём некоторые важные приёмы их описания:
|
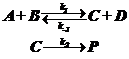
протекает по двум или более путям. Этот принцип чрезвычайно важен при анализе внутримолекулярных процессов типа циклических движений марковских перескоков в виде трёхпозиционного вращения.
См. примеры.
Пример 3.1. Рассмотрим кинетическую схему реакции: 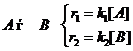
и ту же самую реакцию в присутствие протонов: 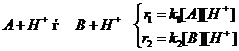
Скорость реакции равна: ![]()
И в условиях равновесия приходим к сомнительному результату вида:
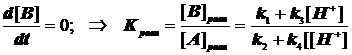 (4.7)
(4.7)
Возникает парадокс, согласно которому константа равновесия, вопреки незыблемым установкам термодинамики, выглядит зависимой от концентрации протонов. Для его устранения вводится принцип детального равновесия. Он состоит в том, что система кинетических уравнений дополняется условиями детального равновесия:
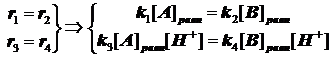 (4.8)
(4.8)
В результате концентрация протонов исчезает из выражения константы скорости, а именно:
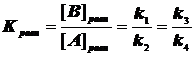 (4.9)
(4.9)
Пример 3.2. Рассмотрим кинетику циклического превращения вида:
Если уравнение скорости реакции включает сумму различных членов для прямой реакции, что указывает на возможность нескольких путей её протекания, то принцип детального равновесия требует, чтобы каждый член в выражении для скорости прямой реакции был скомпенсирован при равновесии соответствующим членом в выражении для скорости обратной реакции.
4) Мономолекулярные реакции. Схема Линдемана.
Существование мономолекулярных реакций типа реакций разложения в газах необычно с точки зрения бимолекулярного механизма накопления энергии активации. Наблюдаемый порядок первый, а стадия активации не может быть иной, как бимолекулярной. В чём же дело? В качестве варианта объяснения этой ситуации Линдеман предложил такие процессы рассматривать как сложные, включая в них следующие стадии:
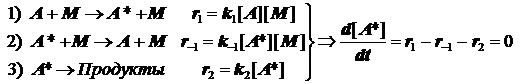 (4.9)
(4.9)
Отсюда следует простой результат.
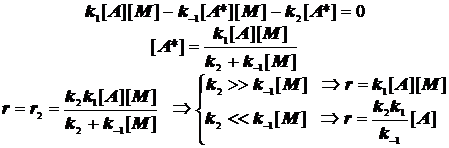 (4.10)
(4.10)
Экспериментальные данные часто не вполне соответствуют простой формально-кинетической схеме Линдемана, однако теоретические уточнения позволяют достичь приемлемого количественного и качественного согласия наблюдаемых фактов с этим механизмом. Всё же в основном идея балансирования между стадиями активации, дезактивации и самого превращения оказывается верна.
Пример 4.1 , илюстрирующий схему Линдемана: Реакция разложения диметилового эфира ![]()
5) О роли газокинетических моделей, из которых вытекают основные воззрения химической кинетики и о доводах в её пользу. (Забегаем немного вперед в части представлений об активации химического процесса).
Смотрите также
Жидкие кристаллы
Некоторое время
тому назад необычной популярностью в США пользовалась новинка ювелирного
производства, получившая название “перстень настроения”. За год было продано 5 0 миллионов таких ...
Равновесия в неводных растворах
...
Магнийорганические соединения
Магнийорганические
соединения относятся к числу одних из самых известных металлоорганических соединений.
Они широко применяются в органическом синтезе, хотя в последнее время их
потеснили л ...