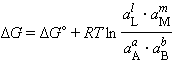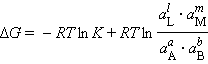Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Химическое равновесиеОткрытая химия / Химическая термодинамика / Открытая химия / Химическая термодинамика / Химическое равновесие Химическое равновесиеСтраница 2
где – стандартный изобарно-изотермический потенциал вещества j;
![]() – его активная концентрация (активность).
– его активная концентрация (активность).
Для идеальных растворов активная концентрация определяется как отношение концентрации этого вещества при заданных условиях к его концентрации в стандартном состоянии a = C/C°. Вещества в стандартном состоянии имеют a = 1.
В соответствии с (4.7) энергия Гиббса произвольной химической реакции
|
aА + bВ = lL + mМ |
равна:
|
(4.8) |
При достижении равновесия (ΔG = 0) уравнение (4.8) принимает вид
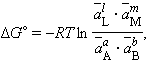 |
где
– равновесные значения активных концентраций.
Выражение под знаком логарифма, представляющее собой отношение произведения равновесных активностей продуктов к произведению активностей исходных веществ в степенях их стехиометрических коэффициентов, называется константой равновесия:
| |
(4.9) |
|
|
|
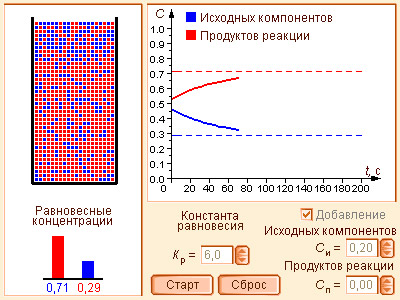
Модель 4.12. Химическое равновесие |
Подставив (4.9) в (4.8), получим уравнение, носящее название изотермы Вант-Гоффа:
|
(4.10) |
Смотрите также
Разработка методики определения ультрамикрограммовых количеств тяжелых металлов методом инверсионной вольтамперометрии
Актуальность.
Современный уровень развития технологии, биологии, медицины, охраны окружающей
среды и других областей науки и техники выдвигает задачу определения малых
количеств веществ во ...
Выводы.
1. Для осаждения препарата
протеиназы целесообразно применять этанол или изопропанол.
2. Компонентный состав препарата
представлен четырьмя фракция ...
Синтез жирных кислот
Синтетические жирные кислоты (далее по тексту – СЖК)
находят широкое применение как заменители пищевых жиров в производстве мыла и
моющих средств, пластификаторов, мягчителей, стабилизаторов ...