Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Кинетическая кислотностьОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Кинетическая кислотность Кинетическая кислотностьСтраница 1
Важной особенностью большинства СН-кислот является относительно низкая скорость отрыва от них протона. В отличие от этого перенос протона между электроотрицательными элементами (О, N) происходит быстро. Так, скорость переноса протона между Н3О+ и ОН- равна 1,4.1011 л/моль.с, что является одной из самых высоких констант скорости бимолекулярных реакций в воде. Протонизация О- и N-оснований под действием Н3О+ или отщепление протона от других ОН- и NH-кислот под действием ОН- происходит на порядок величины медленнее, чем реакция Н3О+ с ОН-. Примеры приведены в табл. 3.16.
Таблица 3.16
Скорости переноса протона в водном растворе при 25оС
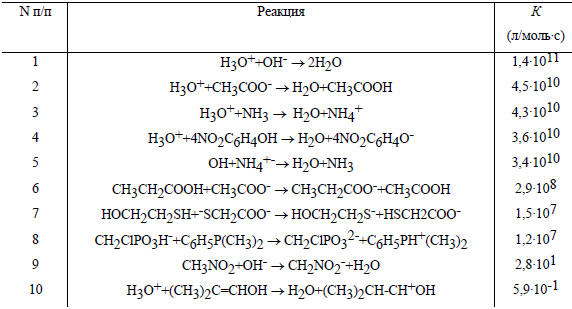
Известно, что ионы Н3О+ и ОН- в водном растворе сильно сольватированы, и перенос протона происходит без предварительного удаления сольватной оболочки по особому механизму, в котором протон смещается по цепочке молекул воды, связанных водородными связями (механизм Гроттгуса):
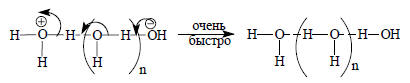
Перенос протона происходит при относительно большом расстоянии между Н3О+ и ОН-. Он должен быть быстрым, так как ионам Н3О+ и ОН- не надо тратить время на сближение друг с другом. Но реакция Н3О+ и ОН- в воде - это особый случай. В большинстве других растворителей взаимодействие донора и акцептора протона происходит при их тесном контакте. Тогда важным фактором становится способность донора и акцептора протона образовывать между собой водородную связь (см. разд. 3.3.3). Еще до начала переноса протона донор и акцептор должны образовывать комплекс с водородной связью, в котором они ориентированы нужным образом. Чем сильнее водородная связь, тем короче будут расстояния, на которое должен смещаться протон, и тем ниже будет барьер реакции. Этот эффект начинает проявляться уже в реакциях № 7 и 8 из табл. 3.16, в которых образуются водородные связи S .H-S или О-Н .Р. Такие связи слабее водородных связей между О и N, и поэтому скорости переноса протона меньше, чем для реакций № 1-6. В случае СН-кислот (реакция № 9) и С-оснований (реакция № 10) скорости переноса протона сильно понижены.
Иногда сильное водородное связывание, наоборот, замедляет перенос протона. Это наблюдается, когда отщепляется протон, являющийся частью внутримолекулярной водородной связи, например, в анионе салициловой кислоты:
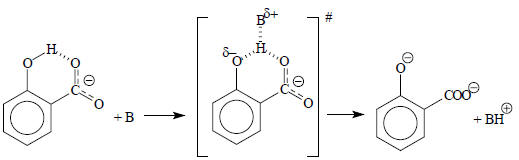
Перенос протона от фенольного гидроксила этого соединения идет в 103 раз медленнее, чем от самого фенола, поскольку в переходном состоянии протон связан с двумя атомами кислорода и атомом В, и поэтому рвущаяся и образующаяся связи не колинеарны, что было бы оптимальным для переноса протона. Энергия такого переходного состояния будет выше, чем в отсутствие внутримолекулярной водородной связи, и, следовательно, скорость реакции будет меньше.
Перенос протона может замедлиться и вследствие пространственных факторов. Например, в 2,6-ди-трет-бутилпиридин (I) реагирует с Н3О+ в 100 раз медленнее, чем незамещенный пиридин. Особенно медленно отщепление протона происходит в том случае, когда имеются и пространственные затруднения, и внутримолекулярная водородная связь. примерами являются 1,8-бис-(диметиламино)-нафталин (II) и особенно его 2,7-диметоксипроизводное (III):
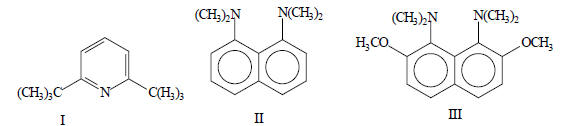
Объемистые группы (CH3)2N выталкивают друг друга из плоскости нафталиновой ароматической системы и получается конформация, в которой неподеленные пары атомов азота направлены почти навстречу друг другу. В результате возникает электростатическое отталкивание и напряжение в остальной части молекулы. Отталкивание и напряжение в значительной степени снимаются при протонизации молекулы:
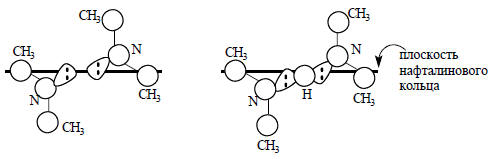
Вследствие этого производные 1,8-(диметиламино)нафталина делаются очень сильными основаниями. Например, для соединения III в воде рКа=16,3 (ср. с рКа других аминов в табл. 3.3). Удалить протон из сопряженных им кислот чрезвычайно трудно. По этой причине 1,8-бис-(диметиламино)нафталин получил название "протонная губка". Еще медленнее происходит отщепление протона от дипротонированной изнутри молекулы [1.1.1]-криптанда (IV): первый протон отщепляется ионом ОН- со скоростью 1,4.10-8 л/(моль.с), а второй протон от монокатиона (V) вообще нельзя удалить без разрушения скелета молекулы:
Смотрите также
Применение органических реагентов в аналитической химии
Органические
вещества широко применяются в аналитической химии вообще и в фармацевтическом
анализе, в частности. Ещё с начала нашей эры было известно, что настой
чернильных дубильных орешко ...
Заключение
29Cu – Медь
[Ar]3d104s1
Древние цивилизации оставили нам множество
изделий из бронзы.
Атомная
масса: 63,54
Электроотрицательность:
1,9
Тпл:
10 ...


