Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Соотношение линейности свободных энергий и структура переходного состоянияОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Соотношение линейности свободных энергий и структура переходного состояния Соотношение линейности свободных энергий и структура переходного состоянияСтраница 2
Возьмем в качестве примера кислотную ионизацию замещенных толуолов под действием оснований В- в сильно основных средах (например, NaNH2/NH3 (жидк.), (C2H5)3NOH, ДМСО и т.п.:
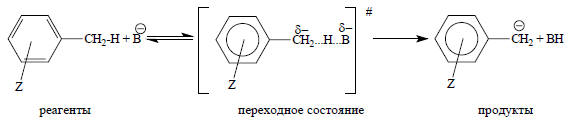
Отрыв протона происходит достаточно медленно, и поэтому скорость этой реакции легко поддается измерению обычными кинетическими методами. Если в реакции переходное состояние "позднее" (как ПСЗ на рис. 3.15), то оно будет подобно продукту реакции ZC6H4CH2-, заместитель Z будет активно участвовать в делокализации заряда, и реакция будет чрезвычайно чувствительна к электрическим эффектам Z что приведет к высокому абсолютному значению |ρ|. Если переходное состояние "раннее" (как ПС1 на рис. 3.15), то в нем отрицательный заряд будет небольшим, реакция будет менее чувствительна к электрическим свойствам заместителя Z , и величина |ρ| будет меньше.
Такую картину иногда называют принципом селективности. Очень реакционноспособный реагент относительно мало селективен в реакции с данным субстратом (|ρ| мало), а реагент с низкой реакционной способностью в этой же реакции очень селективен (|ρ| велико). Таким образом, можно прийти к заключению, что в быстрых реакциях переходное состояние более похоже на реагенты, чем на продукты, а в медленных реакциях наоборот.
Здесь возникает дилемма. Уравнение Гаммета используется для исследования типа переходного состояния (по величине |ρ|) в семействе сходных соединений путем варьирования заместителей, и, следовательно, путем изменения реакционной способности. Но постулат Хэммонда устанавливает, что при изменении скорости неминуемо должна измениться и структура переходного состояния. Проблема в настоящее время остается нерешенной. В основу уравнения Гаммета и постулата Хэммонда заложен противоречивый смысл. Имеющийся огромный экспериментальный материал позволяет утверждать, что гамметовские графики действительно линейны, нередко в интервале изменения скоростей 105-106 раз. Правда, иногда наблюдаются отклонения от линейности, но они обычно объясняются не изменениями структуры переходного состояния, а резкой сменой механизма реакции для определенных заместителей. В некоторых случаях не соблюдается и принцип селективности. Так, в реакциях электрофильного ароматического замещения (гл. 13) Br2 в трифторуксусной кислоте в 106 раз более реакционноспособен, чем Br2 в уксусной кислоте, но в обоих случаях селективность практически одинакова; иногда более реакционноспособные системы имеют более высокие значения ρ, чем менее реакционноспособные.
С другой стороны, во многих реакционных сериях влияние заместителей трудно объяснить без привлечения представлений об изменчивости переходного состояния (например, в реакциях отщепления типа Е2; см. разд. 10.2, гл.10). В целом трудно понять, почему переходное состояние, которое изменяется при относительно небольшом изменении реагентов (что видно из изменения величины |ρ|) может не измениться при подобных же небольших изменениях субстрата (введение заместителя Z).
Возможно, что константы ρ и σ не есть независимые параметры, как предполагается, а связаны между собой, причем параметр, связывающий ρ и σ, в их произведении сокращается. например, если электронодонорный заместитель Z изменяет переходное состояние путем увеличения отрицательного заряда на реакционном центре, то этому заместителю будет труднее отдавать электроны при увеличенном отрицательном заряде т.е. его донорная способность может понизиться. В таком случае структуру переходного состояния можно охарактеризовать величиной хρ где ρ отражает главные черты переходного состояния, а х - его модификацию заместителем. С другой стороны, возможно, что мерой отклика заместителя на изменение переменного переходного состояния является величина σ/х. В произведении х сокращается, и в уравнение Гаммета входит лишь σρ.
Смотрите также
Иод
ИОД (лат. Iodium), I - химический элемент VII группы
периодической системы Менделеева,
относится к галогенам (в литературе встречается также символ J); атомный номер
53, атомная масса 126, ...
Производство глутаминовой кислоты
Глутаминовая кислота (α-аминоглутаровая) является одной из
важнейших аминокислот растительных и животных белков. Не относится к числу
незаменимых, однако, тем не менее, служит основой д ...
Активация малых молекул
В катализе часто применяют термин “активация”,
понимая при этом повышение реакционной способности реагентов. Попытаемся
наполнить этот термин конкретным физическим содержанием. Под активацие ...


