Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Величина и смысл коэффициентов БренстедаОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Величина и смысл коэффициентов Бренстеда Величина и смысл коэффициентов БренстедаСтраница 1
Общий кислотный и общий основной катализ с медленным переносом протона
В типичном случае общего кислотного или общего основного катализа перенос протона от АН к R или от RH к В является самой медленной стадией общего многостадийного процесса (разд. 3.3.6.в). Рассмотрим, например, энергетический профиль реакции для общего основного катализа, когда скорость реакции контролируется переносом протона от реагента RH к катализатору Во (рис. 3.11,а). Энергетический профиль можно представить как результат наложения друг на друга отдельных параболических кривых потенциальной энергии для RH и ВоН+, соответствующих растяжению связи R-H при переходе от (RH+Bo) к переходному состоянию (R .H .Bo) и растяжению связи Во-Н при переходе от (BoH++R-) к этому же переходному состоянию (последний процесс происходит в обратной реакции; (рис. 3.11.б).
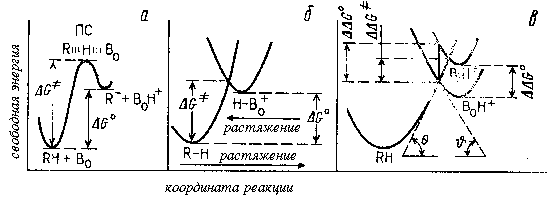
Рис. 3.11. Реакция переноса протона (а), ее моделирование двумя кривыми растяжения связей (б) и вывод соотношения Бренстеда (в)
Теперь изменим катализатор Во на немного более слабое основание Bi. Энергия сопряженной кислоты BiH+ будет немного выше энергии ВоН+, а если Bi и Во не очень отличаются по типу и строению (например, Bi и Во - два замещенных в кольцо анилина; однако нельзя брать случаи, когда, например, Вi=анилин, а Во=СН3О-), то форма двух кривых BH+ будет одинакова, и просто одна парабола будет вертикально сдвинута относительно другой без изменения (рис. 3.11,в). Разность свободных энергий активации ΔΔG# для двух реакций RH+Во и RH+Bi в таким случае будет приблизительно пропорционально разности свободных энергий ΔΔGо для равновесной диссоциации ВоН+ и BiH+. Если представить ветви парабол в области пересечения параллельными прямыми, то из рис. 3.11,в следует:
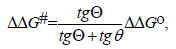
т.е.
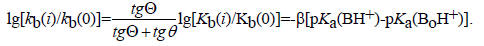
Таким образом, величина коэффициента Бренстеда β (и, аналогично, для кислотного катализа величина α) зависит от наклона кривых для RH и BH+ в точке их пересечения. Как показано на рис. 3.12, величина коэффициента Бренстеда должна лежать в пределах от 0 до 1, т.е.
0≤β≤1 для реакции RH+B → R-+BH+
и
0≤α≤1 для реакции R+АН → RН++А-.
Если кривые пересекаются в вершине параболы RH, то β=0 (рис. 3.12,а), и перенос протона происходит без затраты энергии. Такую реакцию практически реализовать очень трудно, так как при больших скоростях переноса протона лимитирующей стадией может стать процесс образования комплекса соударения RH с В, и наблюдаемая величина практически будет следствием диффузионного контроля, а не характера пересечения энергетических кривых. Следовательно, α→0, β→0, если скорость переноса протона контролируется диффузией реагентов. Если кривые пересекаются в вершине парабола ВН+, то β=1 (рис. 3.12,в). В этом случае реагенты переходят в продукт путем постепенного подъема по склону энергетической поверхности, и "яма" на кривой ВН+ фактически является высшей точкой поверхности. Очевидно, что α→1 (β→1) характерны для очень медленных процессов переноса протона (реакция очень слабых кислот с очень слабыми основаниями).
Наиболее часто в практике встречаются случаи, когда 0<α(β)<1 (рис. 3.12,б).
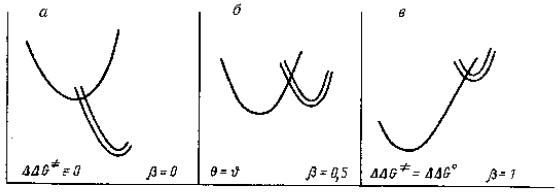
Рис. 3.12. Физический смысл коэффициента Бренстеда. а - tgθ→0; по энергии и структуре переходное состояние (R .H .B) очень близко к реагентам (RH+B). б - обычная реакция. в - переходное состояние очень близко к продуктам реакции (R-+BH+); tgθ→1
Таким образом, величина коэффициента Бренстеда проливает свет на структуру переходного состояния. Если α(β) малы по величине, то структура переходного состояния близка к структуре реагентов, активационного барьера почти нет, и лимитирующей стадией может быть диффузия реагентов друг к другу. Если α(β) приближается к единице, то структура переходного состояния близка к структуре продуктов реакции.
Смотрите также
Источники поступления
В отраслях
промышленности – основными загрязнителями окружающей среды являются:
электроэнергетика – 0,2%, цветная металлургия – 3%, химические и
нефтепромышленные предприятия – 5%, машиностроение и ...
Основы метода потенциометрического
титрования.
Рассмотрим основные
понятия потенциометрического титрования, его виды и методы проведения, способы установления
точки эквивалентности при титровании. ...
Образование сложных эфиров. Некоторые производные углеводов
В
живой природе широко распространены вещества, многим из которых соответствует
формула Сх(Н2О)у. Они представляют собой,
таким образом, как бы гидраты углерода, что и обусловило их названи ...


