Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ВведениеОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Введение ВведениеСтраница 1
Как правило, органические реакции являются сложными многостадийными процессами, состоящими из последовательности простых (элементарных) реакций. Эти элементарные реакции обычно делят на три категории. К первой категории относятся различные изомеризации и перегруппировки, в которых изомер А переходит в изомер В:
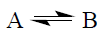
Вторая категория включает рекомбинацию молекул или ионов А и В или диссоциацию молекулы АВ на фрагменты А и В:
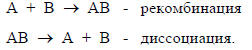
Наконец, к третьей категории относятся бимолекулярные процессы замещения:
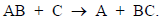
Большинство из перечисленных категорий реакций (кроме некоторых видов изомеризации и процессов диссоциации) начинается с возникновения внутри- и межмолекулярных донорно-акцепторных взаимодействий; диссоциация начинается с ослабления донорно-акцепторного взаимодействия между А и В, существовавшего в молекуле АВ до реакции. В разделе 2.3.2 (гл. 2) мы уже упоминали, что в донорно-акцепторном комплексе акцепторную молекулу можно рассматривать как кислоту, а донорную молекулу - как основание, и следовательно, образование этого комплекса соответствует нейтрализации кислоты основанием. Точно так же любую устойчивую молекулу можно рассматривать как продукт соединения двух фрагментов: кислоты и основания, и если в реакции происходят диссоциация на эти фрагменты, то, по существу, эта реакция является процессом, обратным реакции нейтрализации.
История возникновения и развития представлений о кислотно-основном взаимодействии как основе химических реакций насчитывает более 300 лет. В XVII в. Р.Бойль считал, что кислоты - это тела, атомы которых имеют острые выступы (поэтому они имеют кислый вкус), а основания - это тела, атомы которых имеют поры (вяжущий вкус), и реакция нейтрализации сводится к тому, что выступы кислоты входят в поры основания. В XVIII в. Лавуазье в поисках "кислотной сущности" пришел к выводу, что в кислотах обязательно должен содержаться элемент О (отсюда русское название элемента "кислород", немецкое Sдuerstoff и т.д.). Но Дэви, в течение 15 лет искавший в соляной кислоте кислород, строго доказал, что в HCl кислорода нет. В конце XIX и начале XX вв. господствовала электрохимическая теория кислот и оснований Аррениуса и считалось, что существует только одна кислота - протон и только одно основание - гидроксильный анион, а основные свойства таких молекул, как NH3 можно объяснить тем, что при растворении в воде образуются ионы ОН- и NH4+.
В 1920-х годах практически одновременно Льюис и Бренстед выдвинули свои теории кислот и оснований, которыми в настоящее время пользуются практически все химики. В 1960-х годах Пирсон дополнил теории Льюиса и Бренстеда, предложив использовать представления о "жестких" и "мягких" кислотах и основаниях. Эти представления хорошо обоснованы квантовой химией; таким образом, чисто химические понятия "кислота" и "основание" в настоящее время получили физическое содержание.
Основание Льюиса - это молекула (или анион), которая является донором электронной пары. Как правило, в образовании ковалентной связи с другой молекулой (или катионом) принимает участие несвязывающая (неподеленная) пара электронов основания. Другая молекула (или катион), с которой образует связь основание, является акцептором электронной пары и называется кислотой Льюиса. Обычно кислоты Льюиса первоначально имеют на два электрона меньше числа, соответствующего заполненной валентной оболочке (6 вместо 8). Ниже приведены примеры Льюисовых кислотно-основных реакций:
Смотрите также
Формование изделий из полистирола
Решающим фактором
быстрого развития производства полимерных материалов явилась их конкурентоспособность
с традиционными материалами. И если вначале полимерные материалы
рассматривались как ...
Огнестойкие композиции на основе полибутилентерефталата
"В химии нет отходов, есть только
неиспользованное сырье" Д. И. Менделеев.
Как известно, развитие современной техники
невозможно без исследования пластических масс, в особенност ...
Экспериментальная часть
Измерения
проводили по трехэлектродной схеме: рабочий электрод – стеклоуглеродный
стержень (Æ 0,7 мм), вспомогательный электрод – стеклоуглеродный тигель (V = 25 см3) и электрод сравнения – хл ...


