Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Дисперсная системаСтатьи и работы по химии / Статьи и работы по химии / Дисперсная система Дисперсная системаСтраница 3
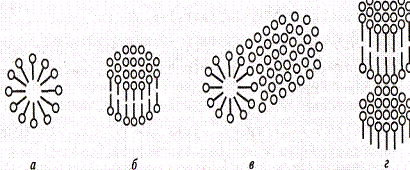
Рис.1. Формы мицелл: а — сферические; 6 — дискообразные; в — цилиндрические; г — пластинчатые
Числа агрегации мицелл обычно равны 20—100, т. е. недостаточно не лики, чтобы можно было считать мицеллу макроскопической фазой. Совокупность мицелл, однако, можно считать «псевдофазой».
Энергетика образования мицелл диктует условия выгодности существования мицелл с некоторой оптимальной степенью диссоциации и оптимальным радиусом, соответствующим приблизительно вытянутой длине углеводородной цепи (несколько меньше). Например, минимальный диаметр мицелл додецилсульфата натрия равен 5,5 нм, а степень диссоциации — 65 (при Т=25°С).
В неводных средах могут возникать обратные мицеллы с ориентации ПАВ, противоположной той, которая существует в водных мицеллах. И кратных мицеллах полярные группы объединяются в гидрофильное ядро, гидрофобные цепи обращены в аполярную среду. Склонность к самодиссоциации в аполярных средах выражена гораздо слабее. Степень диссоциации в обратных мицеллах оказывается значительно меньше (обычно т < 15 , чем в прямых мицеллах, что связано с геометрией молекул, влияющей на энергетическую выгодное именно таких малых мицелл.
62. Определить осмотическое давление гидрозоля золота с массовой концентрацией дисперсной фазы 2 кг/м3 при температуре 293 К, учитывая что диаметр частиц 6·10-9 м, а плотность дисперсной фазы 19,3·103 кг/м3.
Величина осмотического давления определяется только частичной концентрацией (концентрацией дисперсных частиц) и не зависит от их природы и размера. Для разбавленных дисперсных систем осмотическое давление рассчитывается по уравнению, аналогичному уравнению Вант-Гоффа:
![]() ,
,
где ![]() – осмотическое давление, Н/м2;
– осмотическое давление, Н/м2;
γ – массовая концентрация раствора, кг/м3;
М – мицеллярная масса вещества, кг/кмоль.
Для растворов высокомолекулярных соединений частичная масса совпадает с молярной.
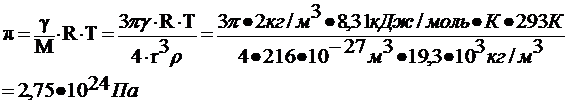
![]()
Ответ: 22,3*1023Па.
77. Адсорбционная хроматография. Уравнения изотермы адсорбции, их анализ и области применения.
Адсорбция – процесс самопроизвольного поглощения вещества (адсорбтива) поверхностью адсорбента. Уравнение Гиббса устанавливает взаимосвязь величины адсорбции (Г, кмоль/кг или кмоль/м 2) с изменением поверхностного натяжения (s, Дж/м2 ) от концентрации раствора (С, кмоль/л). ![]() ,
,
где С – концентрация раствора, кмоль/л;
R – универсальная газовая постоянная;
T – температура;
ds /dС – производная, являющаяся мерой поверхностной активности; может быть определена графически по зависимости поверхностного натяжения от концентрации (при s®0).
Физические процессы молекулярной адсорбции на твердой поверхности описываются уравнениями Ленгмюра и Фрейндлиха.
Уравнение Ленгмюра:
![]() ,
,
где Г – величина адсорбции, кмоль/кг или кмоль/м2;
Гmax – величина предельной адсорбции, кмоль/кг (кмоль/м2);
С – концентрация раствора, кмоль/л;
а – константа равновесия адсорбции.
Это уравнение хорошо описывает адсорбцию для малых и больших концентраций растворов (или давлений газа).
Эмпирическое уравнение Фрейндлиха:
![]() ,
,
где Г – величина адсорбции, кмоль/кг (кмоль/м2);
n – количество вещества-адсорбтива, кмоль;
m – масса адсорбента, кг;
К – константа (при С = 1 моль/л К = Г);
1/а – константа (адсорбционный показатель); зависит от природы адсорбента и температуры. 1/а = 0,1–1.
Уравнение (2.11) хорошо описывает адсорбцию для интервала средних концентраций растворов (или давлений газа).
Адсорбция на жидкой поверхности может приводить как к уменьшению поверхностного натяжения (например, при адсорбции малорастворимых, дифильных поверхностно-активных веществ), так и к его увеличению (в частности, при адсорбции поверхностно-инактивных веществ, т. е. хорошо растворимых в воде неорганических электролитов) или не изменять его (растворы сахаров в воде). В последнем случае вещество распределяется равномерно между поверхностным слоем и объемом раствора.
Смотрите также
Фазовые равновесия в системе MgS-Y2S3
Соединения с участием
РЗЭ остаются по прежнему обширным резервом для создания новых материалов.
Возможно создание материалов с уникальными, заранее заданными свойствами.
Взаимодействие в
...
Введение.
Уравнение
Ван-дер-Ваальса используется при исследовании процессов разделения и является
базовым уравнением при качественном исследовании этих процессов.
Распространение уравнения такого типа на мно ...
Насыщенные альдегиды и кетоны
Альдегиды
и кетоны относятся к карбонильным соединениям (содержат группу >С=О) Они
имеют общую формулу:
для
альдегидов R1=H.
Изомерия
кетонов связана со строением радикалов и с п ...


