Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Кислотно-основной катализСтатьи и работы по химии / Гомогенный катализ / Статьи и работы по химии / Гомогенный катализ / Кислотно-основной катализ Кислотно-основной катализСтраница 3
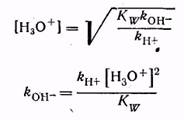
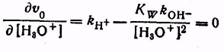 Откуда:
Откуда:
Подставив значение kOH-, получим определяемую опытным путем минимальную скорость; из неё, сравнив уравнение с исходным уравнением для V0, получим:
![]()
т.е. каталитическое действие ионов H3O+ и ОН- в точке минимума одинаково. Эта точка носит название изокаталитической.
Таким образом, изменив условия опыта, можно, согласно дуалистической теории катализа, по экспериментальным данным определить числовое значение кинетических констант, входящих в уравнение скорости.
Что касается первично солевого эффекта, то его можно объяснить на основании теории сильных электролитов Дебая-Гюккеля. Введение соли, не содержащей общих ионов с компонентами смеси, изменяет ионную силу раствора, вследствии чего изменяется степень диссоциации веществ и концентрации катализирующих реакцию частиц.
Смотрите также
Заключение
При написании работы
был изучен метод потенциометрического титрования. В результате можно выделить несколько
основных преимуществ данного метода титрования перед методом кислотно-основного
титрован ...
Концентрирование карбамида
Карбамид (мочевина) СО(NH2)2 представляет
собой амид карбаминовой кислоты.
Карбамид выпускается в виде гранул или
кристаллов. В данном производстве карбамид выпускается в виде ...
Конструирование биосенсора для регистрации P. aeruginosa АТСС 27853
Регистрация патогенных
микроорганизмов в растворах электролитов является одним из основных заданий
медицины, биохимии и электрохимического анализа. С этой целью в мире
разрабатываются биосе ...


