Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Ацилирование ацетоуксусного эфира.Дипломы, курсовые и прочее / Изучение кето-енольной таутомерии на примере АУЭ / Дипломы, курсовые и прочее / Изучение кето-енольной таутомерии на примере АУЭ / Ацилирование ацетоуксусного эфира. Ацилирование ацетоуксусного эфира.
Анионы сложных эфиров взаимодействуют с ацилгалогенидами, образуя продукты ацилирования. Эти реакции осуществляются с наибольшим успехом, если использовать для получения соли енол????????, а гидрид натрия, так как в этом случае не происходит образования спирта, способного реагировать с ацилгалогенидом.
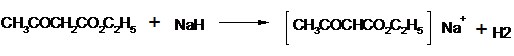
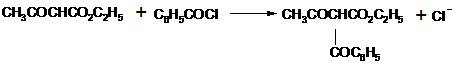
2. Синтезы с АУЭ.
АУЭ широко используется в органическом синтезе. С его помощью можно синтезировать кетоны, модифицировать эфир с образованием различных производных. Целый ряд дополнительных возможностей для синтеза обеспечивают еноляты АУЭ, которые способны подвергаться алкилированию и ацилированию с образованием разнообразных замещенных ацетоуксусного эфира. В отличае от натриймалонового эфира эти реакции могут протекать как по атому гидроксильного кислорода, так и по соседнему углеродному атому. Механзм реакций SN2 в качестве нуклеофила выступает енолят – ион.
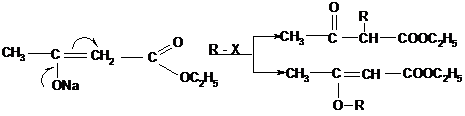
Направление замещения определяется несколькими факторами. Наиболее важным является природа реагента R – X. Чем более мягкой кислотой будет уходящая группа «Х», тем легче будет идти реакция по мягкому реакционному центру – атому углерода. Это и происходит при алкилировании енолята – аниона алкил – йодидами и – бромидами.
Возможности применения АУЭ в синтезах разнообразных продуктов расширяются благодаря его способности подвергаться расщеплению в двух направлениях. При нагревании с разбавленными растворами щелочей или кислот происходит распад образующейся после гидролиза ацетоуксусной кислоты с образованием кетонов. Обработка концентрированными растворами щелочей приводит к образованию из АУЭ двух молекул уксусной кислоты (кислотное расщепление):
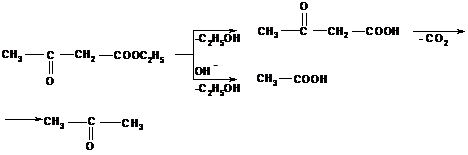
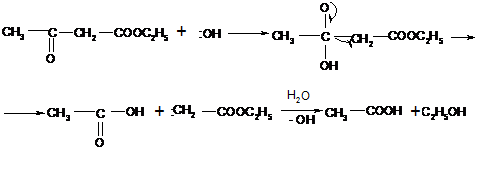
Механизм кислотного расщепления состоит в нуклеофильной атаке гидроксил-ионом карбонильного углерода, несущего частичный положительный заряд. После присоединения гидроксида неустойчивый продукт распадается:
Пример синтеза с использованием АУЭ:
Смотрите также
Определение стабильной и обменной емкости цеолитсодержащей породы Атяшевского проявления
Промышленная
деятельность человека привела к накоплению в природных объектах загрязнений за
счёт пылевидных выбросов и сточных вод предприятий.
В современных
условиях одной из важнейших ...
Дисахариды и полисахариды
В
живой природе широко распространены вещества, многим из которых соответствует
формула Сх(Н2О)у. Они представляют собой,
таким образом, как бы гидраты углерода, что и обусловило их названи ...
Разработка школьного элективного курса "Полимеры вокруг нас"
...


