Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Статический методДипломы, курсовые и прочее / Методы определения активности катализаторов / Дипломы, курсовые и прочее / Методы определения активности катализаторов / Статический метод Статический метод
Реакцию проводят в замкнутом объеме до установления термодинамического равновесия, либо до полного превращения одного из исходных реагентов. Концентрация реагентов меняется от исходной до равновесной, соответственно меняется и скорость реакции по закону действующих масс (основному закону кинетики). В исследуемом объеме при отсутствии диффузионных торможений и постоянстве температуры имеют место соотношения [1]
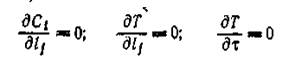 (3)
(3)
где Ci — концентрация компонента реакционной смеси; Т —температура; lj — пространственные координаты реакционной системы; — время.
Часто статический метод используют для измерения скоростей реакций, приводящих к изменению числа молекул, что позволяет следить за ходом реакции по изменению давления. На рис. 1 дана установка для изучения скорости реакции водорода с кислородом статическим методом. Перед опытом в ней устанавливают вакуум 10-5 мм рт. ст. В процессе реакции через определенные промежутки времени измеряют давление, по изменению которого рассчитывают скорость реакции.[1]
Основным преимуществом статического метода является возможность работы с очень малым количеством исходных веществ и с катализатором в любой форме, а также получение всей кинетической кривой в одном опыте, высокая чувствительность и точность измерений. Однако правильность выводов из результатов, полученных этим методом, зависит, от справедливости допущения квазистационарного протекания реакции. Статический метод рекомендуется применять в тех случаях, когда изменение состава реакционной смеси заметно не сказывается на составе и активности поверхности катализатора и когда изменение состава поверхности катализатора происходит гораздо быстрее, чем реакция.[1]
Вариантом статического метода является проведение реакций в жидкой фазе (например, гидрирование органических веществ). Из-за невысокой чувствительности метода (в отличие от статического метода в газовой фазе) обычно используют катализатор в виде зерен, порошков, но не в виде пленок или нитей. Чувствительность этого варианта статического метода значительно ниже, чем при проведении реакций в газовой фазе.[1]
К недостаткам статического метода следует отнести его интегральный характер (т. е необходимость проводить дифференцирование опытных данных),' возможные перепады температур и концентраций и ряд других. Поэтому указанный метод в настоящее время находит весьма ограниченное применение при изучении активности промышленных катализаторов.[1]
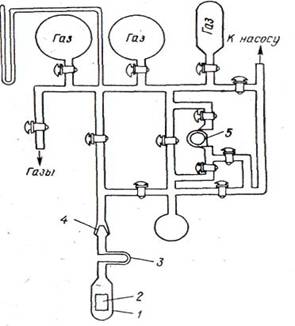
Рис. 1. Установка для изучения скорости взаимодействия водорода с кислородом: 1—контактный кварцевый аппарат; 2 —палладиевая пластинка; 3 — U-образная трубка для вымораживания ртути и паров смазки; 4—шлиф; 5—капилляр.
Смотрите также
Введение.
Уравнение
Ван-дер-Ваальса используется при исследовании процессов разделения и является
базовым уравнением при качественном исследовании этих процессов.
Распространение уравнения такого типа на мно ...
Cупрамолекулярная химия
Проанализировано развитие области науки, называемой
супрамолекулярной химией. Даны основные определения и понятия этой дисциплины.
В историческом контексте рассмотрены исследования, заложивш ...
Концентрация растворов.
Цель работы - приобретение
навыков приготовления растворов различной концентрации из сухой соли или более
концентрированного раствора.
Приведем
несколько примеров расчета по теме "Концент ...


