Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Расчет и построение равновесной диаграммы потенциал – pH для
системы Cu – H2OДипломы, курсовые и прочее / Равновесные и поляризационные диаграммы потенциал-pH / Дипломы, курсовые и прочее / Равновесные и поляризационные диаграммы потенциал-pH / Расчет и построение равновесной диаграммы потенциал – pH для
системы Cu – H2O Расчет и построение равновесной диаграммы потенциал – pH для
системы Cu – H2OСтраница 3
На диаграмме можно выделить 5 областей преобладания фаз различного состава. Область I – область иммунности меди, при данных значениях потенциалов и рН медь коррозии не подвергается. Область II – область активной коррозии, в которой медь переходит в раствор в виде катионов Cu2+. Области III, IV – области пассивации, на поверхности меди образуется защитная пассивирующая плёнка, состоящая из оксида Cu2O (область III) и CuO (область IV) Область V – область перепассивации. Линии a и b на диаграмме определяют область электрохимической устойчивости воды.
Данная диаграмма построена без учета существования Cu в данной системе в виде анионов.
Ниже приведены дополняющие картину системы уравнений реакций:
(VIII) HCuO2- + H+ = CuO + H2O pH = 18,83 + lg![]()
(IX) Cu2O3 +H2O + 2ē = 2HCuO2- φ = ?
(X) 2HCuO2- + 4H+ + 2ē = Cu2O +3H2O φ = 1,783 – 0,1182pH + 0,0591·lg![]()
(XI) CuO22- + H+ = HCuO2- pH = 13,15 + lg![]()
(XII) 2CuO22- + 6H+ + 2ē = Cu2O + 3H2O φ = 2,560 – 0,1773pH + 0,0591·lg![]()
(XIII) Cu2O3 + H2O + 2ē = 2CuO22- + 2H+ φ = ?
(XIV) CuO22- + 4H+ + 2ē = Cu + 2H2O φ = 1,515 – 0,1182pH + 0,0295·lg![]()
Аналогично расчетам для уравнений реакций (I) – (VII) для реакций (IX) и (XIII) получаем:
φ(IX) = 0,0309 –0,0591·lg![]()
φ(XIII) = –0,759 + 0,0591pH + 0,0591·lg![]()
Для системы Cu – H2O построена дополненная диаграмма потенциал – pH:
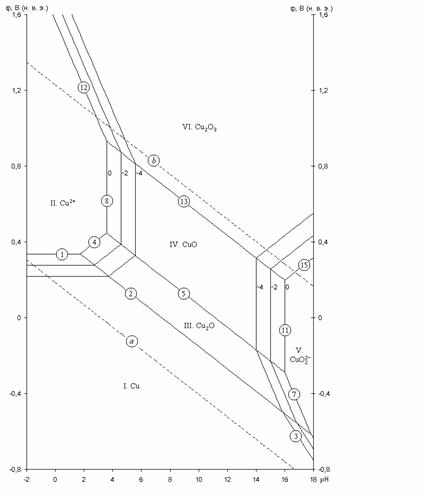
Рис. 2.2 - Равновесная диаграмма потенциал – pH для системы Cu – H2O с учетом существования Cu в виде анионов
На данной диаграмме показаны все условия перехода меди из одних состояний в другие. Можно заметить, что в очень кислой среде пассивирующая пленка меди разрешается, вследствие чего медь вновь переходит в раствор, но на этот раз уже в виде анионов HCuO2- и CuO22-. Отсюда можно сделать вывод, что медь неустойчивак коррозии при высоких значениях pH.


