Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Окислительно-восстановительные реакции органических веществДипломы, курсовые и прочее / Дипломы, курсовые и прочее / Окислительно-восстановительные реакции органических веществ Окислительно-восстановительные реакции органических веществСтраница 6
анодный процесс:
Zn – 2e- = Zn2+;
катодный процесс: в кислой среде –
2Н+ + 2е- = Н2↑;
в нейтральной среде –
1/2О2 + Н2О + 2е- = 2ОН-.
286. Вычислить рН 0,001 М раствора фтористоводородной кислоты и 0,00001 М раствора гидроксида натрия.
Решение:
Электролиты HF и NaOH есть сильными и потому в растворе диссоциируют полностью.
Для указанных растворов имеем:
![]()
![]()
![]()
![]()
Ответ: 3 и 9.
312. Слили 30 г 2 %-ного раствора ацетата свинца Pb(CH3COO)2 и 50 мл 1 М раствора иодоводородной кислоты HI. Определите массу осадка иодида свинца.
Решение:
Уравнение реакции:
![]()
в уравнении ![]() .
.
Теперь рассчитаем какой реагент в избытке:
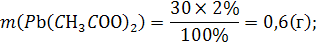
![]() =
=![]()
![]()
– находится в избытке, расчеты ведем по
![]() ; так как
; так как ![]() , то
, то
![]()
Ответ: ![]() .
.
337. В 70 г бензола С6Н6 растворено 2,09 г некоторого вещества. Раствор кристаллизуется при 4,250С. Установить молекулярную массу растворенного вещества. tкрист.бензола= 5,50С.
Решение:
Криоскопическая константа выражается формулой
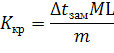
где Ккр – криоскопическая константа; ![]() – величина, получаемая опытным путем – понижение точки замерзания раствора, состоящего из т кг растворенного неэлектролита и L кг растворителя; М – масса 1 моль неэлектролита, кг. Криоскопическая константа бензола Ккр = 5,1°.
– величина, получаемая опытным путем – понижение точки замерзания раствора, состоящего из т кг растворенного неэлектролита и L кг растворителя; М – масса 1 моль неэлектролита, кг. Криоскопическая константа бензола Ккр = 5,1°.
Отсюда
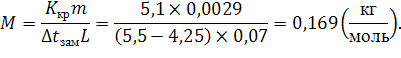
Ответ: ![]() .
.
Смотрите также
Алкадиены. Каучук
Алкадиены, или диеновые углеводороды, — непредельные углеводороды,
содержащие в углеродной цепи молекулы две двойные связи.
...
Определение молярной массы диоксида
углерода.
Цель работы - нахождение
молярной массы диоксида углерода по плотности газа на основе уравнения
Менделеева Клапейрона.
Молярная масса -
это масса одного моля вещества. Моль любого газообразног ...


