Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Окислительно-восстановительные реакции органических веществДипломы, курсовые и прочее / Дипломы, курсовые и прочее / Окислительно-восстановительные реакции органических веществ Окислительно-восстановительные реакции органических веществСтраница 4
143. При сгорании 1 л бутана С4Н10 выделилось 119,1 кДж теплоты. Вычислить энтальпию образования бутана. Условия нормальные.
Решение:
Уравнение реакции:
![]()
![]() ;
;
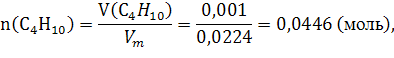
При сгорании ![]()
![]() выделяется
выделяется ![]() теплоты, а при сгорании
теплоты, а при сгорании ![]()
![]() –
– ![]() теплоты, тогда
теплоты, тогда
119,2/2=x/0,0446;
x=2,65 (кДж).
Ответ: выделится ![]() .
.
162. Возможно ли при 2000С протекание следующей реакции:
СО + 0,5О2 = СО2?
Решение:
Возможно ли при 2000С протекание следующей реакции: СО + 0,5О2 = СО2?
О принципиальной возможности и направлении процесса позволяют судить величина и знак ΔG (энергия Гиббса).
ΔG = ΔH – TΔS,
![]()
![]() где ΔH – изменение энтальпии реакции; ΔS – изменение энтропии реакции; Т – температура.
где ΔH – изменение энтальпии реакции; ΔS – изменение энтропии реакции; Т – температура.
![]() - стандартная энтальпия образования вещества
- стандартная энтальпия образования вещества
- стандартная энтропия образования вещества
п - количество вещества
|
СО (газ) |
О2 (газ) |
СО2 (газ) | |
|
|
-110,5 |
0 |
-393,5 |
|
|
197,9 |
205 |
213,6 |
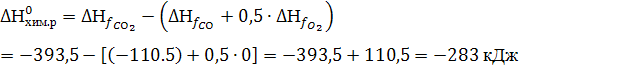
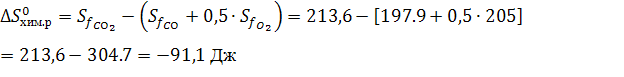
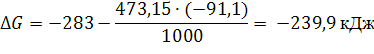
При ΔG<0 реакция самопроизвольно протекает в прямом направлении.
Ответ: возможно, так как ![]() – отрицательная величина.
– отрицательная величина.
189. Температурный коэффициент скорости реакции равен 3. Как изменится скорость реакции, протекающей в газовой фазе, при повышении температуры от 140 до 1700?
|
Дано: |
Решение: Согласно правилу Вант-Гоффа при повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два - четыре раза. Уравнение, которое описывает это правило следующее:
где Отсюда:
|
|
γ = 3 Т1 = 140о Т2 = 170о | |
|
|
Смотрите также
Галогены
Галогены (солероды) – фтор F, хлор Cl , бром Br, йод I и астат At расположены в главной подгруппе VII группы периодической системы
элементов Д.И.Менделеева. Все галогены, кроме астата, вст ...
Прикладная фотохимия
Фотохимия - наука о химических превращениях
веществ под действием электромагнитного излучения: ближнего ультрафиолетового
(~ 100-400 нм), видимого (400-800 нм) и ближнего инфракрасного (0,8 ...


