Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Термодинамический анализ основной реакцииДипломы, курсовые и прочее / Синтез циклогексанона / Дипломы, курсовые и прочее / Синтез циклогексанона / Термодинамический анализ основной реакции Термодинамический анализ основной реакцииСтраница 5
4.7. На основании полученных данных построим графики:
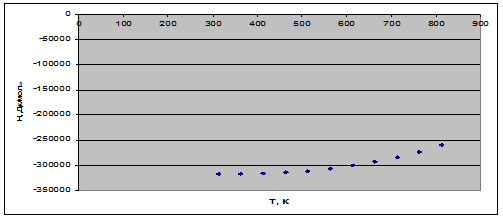
Рис. 1. Зависимость теплового эффекта реакции от температуры.
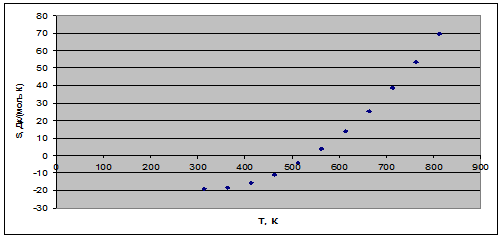
Рис. 2. Зависимость энтропии реакции от температуры.
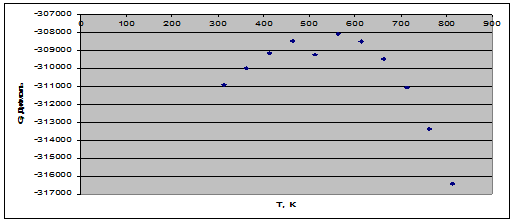
Рис. 3. Зависимость энергии Гиббса от температуры.
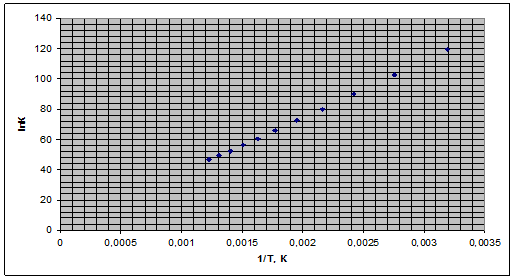
Рис. 4. Зависимость логарифма константы равновесия от обратной температуры.
![]()
![]()
![]()
![]()
613 – -299995,0714
х– -299304
![]() К
К
Выводы:
Рассчитав термодинамические величины, получили:
1) Реакция является экзотермической на всем температурном интервале, т.к. ![]() .
.
2) Для проведения процесса оптимальной считается температура 3390С (612 К).
3) С увеличением температуры изменение энтропии в ходе процесса увеличивается.
4) На всем температурном интервале ![]() , следовательно, реакция идет самопроизвольно.
, следовательно, реакция идет самопроизвольно.
5) Кр>>1, следовательно, реакция смещена в прямом направлении (в сторону образования продуктов), т.к. Кр больше 1020 реакция является необратимой.
Смотрите также
Теоретические основы электрохимической коррозии
Металлы
составляют одну из основ цивилизации на планете Земля. Их широкое внедрение в
промышленное строительство и транспорт произошло на рубеже XVIII-XIX веков. В
это время появился первый ...
Особенности сорбционного извлечения палладия (II) из хлоридных растворов волокнами ЦМ-А2, Мтилон-Т и ВАГ
Одним из
перспективных направлений в комплексном решении экологических проблем является
разработка высокоэффективных процессов очистки промышленных газовоздушных
выбросов, сточных вод и сре ...
Основания
Химия сегодня прочно
вошла в нашу жизнь вместе с новыми материалами, продуктами, лекарствами, синтетическими
волокнами, пластиками. В мире появляется все больше информации о новых веществах
...


