Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Типы гальванических элементовОткрытая химия / Химические источники тока / Открытая химия / Химические источники тока / Типы гальванических элементов Типы гальванических элементовСтраница 2
Схему аккумулятора можно изобразить так:
|
Анодный процесс работающего аккумулятора
| |
катодный процесс –
| |
Таким образом, в свинцовом аккумуляторе осуществляется реакция
| |
При зарядке протекает обратная реакция и электроды меняют свои функции: катод становится анодом, а анод – катодом. ЭДС свинцового аккумулятора зависит от отношения активности кислоты и воды:
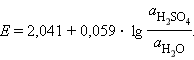 |
В процессе работы аккумулятора концентрация кислоты падает, а следовательно, падает и ЭДС. Когда ЭДС достигает 1,85 В, аккумулятор считается разрядившимся. При более низкой ЭДС пластины покрываются тонким слоем PbSO4 и и аккумулятор разряжается необратимо. Во избежание этого аккумулятор периодически подзаряжают.
В заряженном щелочном железо-никелевом аккумуляторе анодом служит железо, катодом – гидроксид никеля (III), электролит – 20%-й раствор KOH:
|
При работе аккумулятора на аноде происходит окисление железа:
| |
на катоде – восстановление гидроксида никеля (III):
| |
Суммарная активность процесса:
| |
В уравнении Нернста для данного аккумулятора под знаком логарифма стоят не концентрации, а произведения растворимости ПР участвующих в этой реакции труднорастворимых веществ:
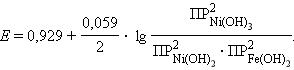 |
Смотрите также
Потенциометрическое титрование и обработка результатов.
Общие
указания при потенциометрическом титровании применимы для большинства
потенциометрических титрований, но в отдельных случаях можно вносить небольшие
изменения.
1. &n ...
Синтез 9-ортогидроксиаминоакридина
Одним из наиболее
перспективных и важных направлений в области медицинской химии является поиск
новых иммуностимуляторов, веществ обладающих противовирусной активностью. К
числу веществ, об ...


