Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Химическое равновесие. Константа химического равновесияДипломы, курсовые и прочее / Энтальпия и ее отношение к теплоте химической реакции. Типы химических связей / Дипломы, курсовые и прочее / Энтальпия и ее отношение к теплоте химической реакции. Типы химических связей / Химическое равновесие. Константа химического равновесия Химическое равновесие. Константа химического равновесияСтраница 2
Т.о., константа равновесия есть отношение констант скорости прямой и обратной реакции. Отсюда вытекает физический смысл константы равновесия: она показывает, во сколько раз скорость прямой реакции больше скорости обратной при данной температуре и концентрациях всех реагирующих веществ, равных 1 моль/л.
Теперь рассмотрим (с некоторыми упрощениями) более строгий термодинамический вывод выражения для константы равновесия. Для этого необходимо ввести понятие химический потенциал. Очевидно, что величина свободной энергии системы будет зависеть как от внешних условий (T, P или V), так и от природы и количества веществ, составляющих систему. В случае, если состав системы изменяется во времени (т.е. в системе протекает химическая реакция), необходимо учесть влияние изменения состава на величину свободной энергии системы. Введем в некоторую систему бесконечно малое количество dni молей i-го компонента; это вызовет бесконечно малое изменение термодинамического потенциала системы. Отношение бесконечно малого изменения величины свободной энергии системы к бесконечно малому количеству компонента, внесенному в систему, есть химический потенциал μi данного компонента в системе:
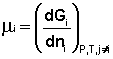 (I.85)
(I.85)
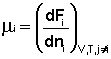 (I.86)
(I.86)
Химический потенциал компонента связан с его парциальным давлением или концентрацией следующими соотношениями:
![]() (I.87)
(I.87)
![]() (I.88)
(I.88)
Здесь μ°i – стандартный химический потенциал компонента (Pi = 1 атм., Сi = 1 моль/л.). Очевидно, что изменение свободной энергии системы можно связать с изменением состава системы следующим образом:
![]() (I.89)
(I.89)
![]() (I.90)
(I.90)
Поскольку условием равновесия является минимум свободной энергии системы (dG = 0, dF = 0), можно записать:
![]() (I.91)
(I.91)
В закрытой системе изменение числа молей одного компонента сопровождается эквивалентным изменением числа молей остальных компонентов; т.е., для приведенной выше химической реакции имеет место соотношение:
![]() (I.92)
(I.92)
Отсюда можно получить следующее условие химического равновесия в закрытой системе:
![]() (I.93)
(I.93)
В общем виде условие химического равновесия можно записать следующим образом:
![]() (I.94)
(I.94)
Выражение (I.94) носит название уравнения Гиббса – Дюгема. Подставив в него зависимость химического потенциала от концентрации, получаем:
![]() (I.95)
(I.95)
Поскольку Σniμi
= ΔF
, а Σniμ°i
= ΔF°
, получаем:
![]() (I.96)
(I.96)
Для изобарно-изотермического процесса аналогичным образом можно получить:
![]() (I.97)
(I.97)
Полученные нами выражения I.96 – I.97 есть изотерма химической реакции. Если система находится в состоянии химического равновесия, то изменение термодинамического потенциала равно нулю; получаем:
![]() (I.98)
(I.98)
![]() (I.99)
(I.99)
Смотрите также
Ознакомление с некоторыми операциями
лабораторной практики и измерительными приборами.
Цель
работы - ознакомление студентов с взвешиванием, измерением объемов жидкостей,
титрованием и др., а также с некоторыми химическими и измерительными приборами.
При подготовке к
выполнению ла ...
Расчет двух ректификационных установок непрерывного действия для разделения смеси этилацетат – толуол
Ректификация -
массообменный процесс, который осуществляется в большинстве случаев в
противоточных колонных аппаратах с контактными элементами (насадки, тарелки),
аналогичными используемыми ...
Источники возбуждения и атомизации в спектральном анализе
Атомизацию, как источник возбуждения, используют в атомно-адсорбционной
спектроскопии. Существует много способов атомизации соединений , осуществляемых
в большинстве случаев за счет тепловой ...


