Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Результаты и их обсуждение.Статьи и работы по химии / Алкилирование енаминов, бета-дикетонов и енаминокетонов / Статьи и работы по химии / Алкилирование енаминов, бета-дикетонов и енаминокетонов / Результаты и их обсуждение. Результаты и их обсуждение.
Из описанных выше реакций С-алкилирования наилучшим образом изучены реакции алкилирования b-дикетонов и енаминов. По енаминокетонам, несмотря на их широкое применение в синтезе, данных значительно меньше. Практическая потребность в проведении алкилирования и обнаруженная неоднозначность протекания этой реакции потребовали ее более детального изучения на конкретных соединениях. В качестве алкилирующего реагента был избран бензилхлорид, в условиях реакции не дающий продуктов полиалкилирования (метилирование в тех же условиях может быть четырех-пятикратным [14]).
Схема проведенных превращений такова:
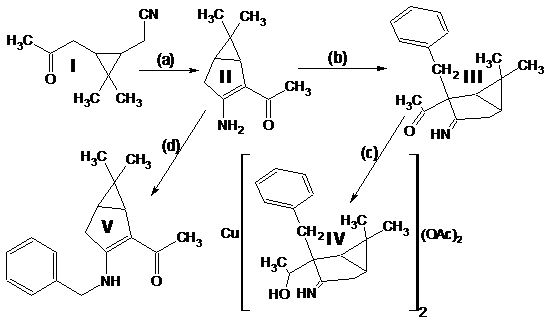
Кетонитрил I
(исходное соединение, чистота ~90% (ГЖХ), предоставлен ЛТС НИОХ СО РАН) является производным природного терпена – 3-карена, выделяемого из соснового скипидара:
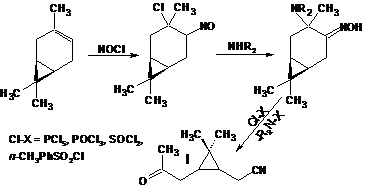
Результирующее соединение IV используется далее в синтезе оптически активных комплексных соединений, используемых в асимметрическом катализе.
Кетонитрил I
представляет собой вязкую темную жидкость, растворимую в органических растворителях и нерастворимую в воде. Реакция (а) проходит гладко и с высоким выходом (~80%) дает продукт конденсации – (3-амино-6,6-диметилбицикло[3.1.0]гекс-2-ен-2-ил)метилкетон II
.
Отдельного рассмотрения заслуживает процесс бензилирования соединения II
. Эта реакция при комнатной температуре протекает крайне неоднозначно, с выходом целевого продукта менее 10% и образованием трудноразделимой смеси изомерных продуктов и продуктов полиалкилирования. Схема превращений и идентифицированные продукты представлены на следующем рисунке:
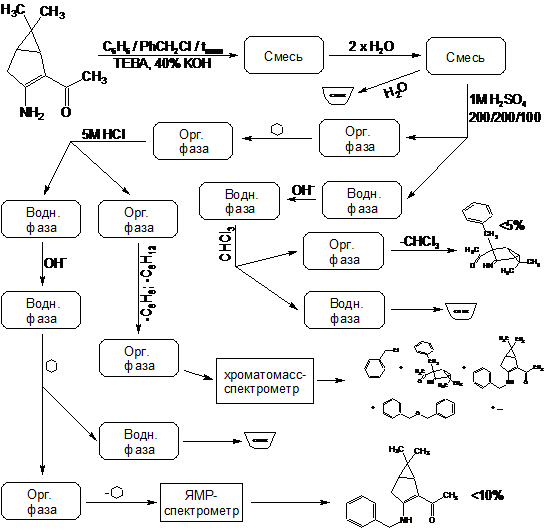
Показанные на схеме процессы обладают повторяемостью – по данным тонкослойной хроматографии в продуктах нескольких проведенных реакций набор компонентов один и тот же. Выходы выделенных веществ тоже примерно одинаковы. Спектры ядерного магнитного резонанса N-алкилированого продукта имеются в Приложениях. Его выход составляет 10%, но (!) – зимой. В тех же реакциях, осуществленных летом, продукт N-алкилирования зафиксирован не был.
Предположение о связи направления алкилирования с температурой реакционной смеси (а в методике указана комнатная температура) подтвердилось – проведение реакции при 35ºС дало в качестве преобладающего продукта (с выходом ~60%) целевой С-замещенный енаминокетон, алкилирование прошло так, как описано в “летней” методике. Попытки дальнейшего повышения температуры пока не предпринимались.
Полученный (3-амино-2-бензил-6,6-диметилбицикло[3.1.0]гекс-2-ил)метилкетон III
был введен в реакцию с избытком боргидрида натрия для восстановлния карбонильной группы в спиртовую.
Точный состав и строение комплекса IV
неизвестны – парамагнитный ион меди II
препятствует получению спектров ЯМР, по данным ИК-спектра что-либо определенное сказать затруднительно. Сводка полученных характеристик соединений дана ниже:

Результаты проделанной работы можно суммировать следующим образом:
- синтезированы и охарактеризованы спектрально и хроматографически некоторые производные природного терпена 3-карена.
- обнаружена значительная зависимость хода реакции бензилирования (3-амино-6,6-диметилбицикло[3.1.0]гекс-2-ен-2-ил)метилкетона от температуры реакционной смеси. Установлено, что оптимальный выход С-бензилированного производного достигается при t≥35˚C.
- установлен тот факт, что “комнатная” температура – весьма ненадежная характеристика методики синтеза.
Смотрите также
Синтез жирных кислот
Синтетические жирные кислоты (далее по тексту – СЖК)
находят широкое применение как заменители пищевых жиров в производстве мыла и
моющих средств, пластификаторов, мягчителей, стабилизаторов ...
Вслед за Либихом
В 1825 г. торговое судно впервые
доставило в Гамбург чилийскую селитру.
Груза было много — он был
насыпан выше бортов, и никто не догадывался, зачем он нужен.
В то время был уже огромн ...


