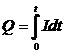Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Методы
исследования процесса растворенияУчим химию / Разработка методики определения ультрамикрограммовых количеств тяжелых металлов методом инверсионной вольтамперометрии / Анализ
следовых количеств веществ и электрохимические инверсионные методы / Учим химию / Разработка методики определения ультрамикрограммовых количеств тяжелых металлов методом инверсионной вольтамперометрии / Анализ
следовых количеств веществ и электрохимические инверсионные методы / Методы
исследования процесса растворения Методы
исследования процесса растворения
Принцип накопления вещества и последующего его электрохимического растворения не является новым; он был, например, использован для измерения толщины металлических пленок. Збинден [4] уже в 1931 г. определял следовые количества меди, осаждая ее на платиновом электроде и измеряя зависимость анодного тока от времени при соответствующем постоянном потенциале в процессе растворения пленки металла.
В пятидесятых годах прием электролитического накопления и последующего электрохимического растворения вещества был распространен на многие электрохимические методы. Наибольшую известность получила вольтамперометрия с линейным изменением потенциала во времени [5 – 7] в связи с ее методической и инструментальной простотой.
Осциллографическая полярография [8] (рабочий электрод поляризуется переменным током с постоянной плотностью, амплитудой и частотой, а на экране осциллографа регистрируется функция dj/dt = f(j), квадратноволновая полярография [9] и переменнотоковая полярография [10], хронопотенциометрия и кулонометрия [11 – 13] могут быть также использованы для исследования процесса растворения. В некоторых случаях для повышения чувствительности определения применяют нестационарные методы. Для исследования процесса электрохимического растворения используются, таким образом, любые методы, основанные на изучении стационарных и нестационарных поляризационных кривых (табл. 1.3).
Таблица 1.3. Методы, применяемые при исследовании инверсионного процесса 3
|
Контролируемый параметр |
Измеряемая функция |
Название метода |
|
Стационарные методы | ||
|
j |
I = f(j) |
Вольтамперометрия при постоянном потенциале |
|
j |
|
Кулонометрия при постоянном потенциале |
|
j |
Q = f(c) |
Полярографическая кулонометрия |
|
I |
Q = It |
Кулонометрия при постоянном токе |
|
Нестационарные (потенциостатические) методы | ||
|
j |
I = f(t) |
Хроноамперометрия |
|
j = ji + wt |
I = f(j) |
Полярография и вольтамперометрия с переменным потенциалом (single sweep, multi-sweep) |
|
j + j(t) |
I(t) = f(j) |
Полярография и вольтамперометрия с наложением переменного напряжения (переменнотоковая полярография квадратноволновая полярография, импульсная полярография) |
|
Нестационарные (гальваностатические) методы | ||
|
I |
j = f(t) |
Хронопотенциометрия |
|
I + I sinwt |
|
Осциллографическая полярография с переменным током |
Смотрите также
Получение метана и опыты с ним
...
Обмен углеводов
Биосинтетические процессы,
протекающие в клетках, нуждаются не только в энергии, им необходимы также
восстановительные эквиваленты в виде НАДФН+Н + и целый ряд
моносахаридов, имеющих в свое ...