Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Процессы, механизмы и кинетические модели в синтетической химииУчим химию / Учим химию / Процессы, механизмы и кинетические модели в синтетической химии Процессы, механизмы и кинетические модели в синтетической химииСтраница 1
Окислительная димеризация алкинов (реакция Глязера-Залькинда) занимает важное место в синтетической химии.
![]()
В этой реакции, в отличие от Вакер-процесса, оба компонента каталитической системы Cu(I) и Cu(II) принимают участие в образовании продукта, а О2 (или другой окислитель, Q, Fe(CN)63– и т.д.) регенерирует необходимую для реакции форму Cu(II). Дегидроконденсацию алкинов можно провести в электрохимической системе (в анодной камере электролизера), например, по реакции
![]()
При использовании в качестве окислителя Cu(OAc)2 в Ру реакция является автокаталитической. В системе CuCl-CuCl2-LiCl-H2O при большом избытке LiCl (т.е. при постоянной концентрации Cl–) скорость димеризации метилацетилена описывается уравнением
![]()
свидетельствующем о наличии лимитирующей стадии и аниона RCºC– в переходном состоянии лимитирующей стадии
[(RCºC–)·2Cu(I)·Cu(II)]≠
Таким образом, продукт превращения интермедиата RCºCCu·CuCl в реакции с CuCl2 (Х1) и является интермедиатом, участвующим в образовании диалкина. Предполагается следующая схема реакции:
![]()
![]()
![]()
![]()
Образование радикала RCºC· в стадии (с его последующей димеризацией) не проходит по термохимическим соображениям. В Мерокс-процесе стадия с участием RS· возможна. Похожая на реакцию димеризации HCN также осуществляется в растворах Cu(I)-Cu(II)
![]()
Гидролиз дициана дает оксамид NH2COCONH2 – очень ценное удобрение.
Синтез оксида этилена. Этиленоксид (ЭО) получают по реакции
![]()
на серебряных катализаторах 15% Ag/a-Al2O3 при 240 – 270оС и давлении 3МПа. При конверсии этилена < 10% селективность 80 – 85%. Побочная реакция – глубокое окисление этилена до СО2. Селективность процесса повышают добавками Cl (NaCl) в катализатор или добавками дихлорэтана в сырье в количестве 2 – 10 ppm. СО2 образуется из С2Н4 и при окислении ЭО, поэтому химизм процесса определяется совокупностью параллельно-последовательных реакций
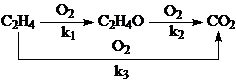
Обсуждаются различные гипотезы о механизме процесса, предполагающие образование СО2 на тех же центрах ZO2, на которых образуется ЭО, или участие разных центров в образовании ЭО (ZO2) и СО2 (ZO). Скорость расходования О2 в области PC2H4 > 0.9 атм на промотированном хлором катализаторе описывается уравнением первого порядка по РО2 (лимитирует адсорбция О2). При РО2 > 0.5 атм и PC2H4 ≤ 0.02
![]()
Смотрите также
Определение степени полимеризации целлюлозы
Молекулярная масса целлюлозы является одной из
важнейших ее характеристик и в значительной степени определяет как области
практического использования различных препаратов целлюлозы, так и
ф ...
Получение метана и опыты с ним
...
Место реакции Белоусова-Жаботинского в химии и современной науке
Автоколебательная
реакция Белоусова-Жаботинского очень широко известна не только в научном мире.
Ее знают как школьники и студенты, так и просто любознательные люди. Стакан с
красно-лиловой ...


