Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Необратимые реакцииСтатьи и работы по химии / Активность. Порядок реакций / Статьи и работы по химии / Активность. Порядок реакций / Необратимые реакции Необратимые реакции
Для реакции первого порядка ![]() , где С – концентрация реагирующего исходного вещества. С другой стороны,
, где С – концентрация реагирующего исходного вещества. С другой стороны, ![]() .
.
![]() ;
;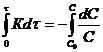 ;
;![]() ;
;![]() (2)
(2)
Из (2) следует, что константа скорости реакции первого порядка не зависит от способа выражения концентрации и имеет размерность ![]() :
:
![]() (3)
(3)
Из уравнения (3) следует, что график в координатах ![]() будет прямой линией:
будет прямой линией:
Уравнение (2) часто записывают в виде ![]() . Для характеристики скорости реакции часто пользуются величиной, называемой временем полупревращения (периодом полураспада), обозначаемой
. Для характеристики скорости реакции часто пользуются величиной, называемой временем полупревращения (периодом полураспада), обозначаемой ![]() - это время, в течение которого испытывает превращение половина взятого исходного вещества. Найдем выражение для
- это время, в течение которого испытывает превращение половина взятого исходного вещества. Найдем выражение для ![]() .
.
В выражение (2) подставляем ![]() :
: 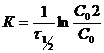 ,
, ![]()
Для реакции 1-го порядка время полупревращения не зависит от начальной концентрации.
Часто в кинетические уравнения подобного вида вводят величину Х, которая характеризует количество вещества, вступившего в реакцию, тогда ![]() и
и ![]() .
.
![]() ;
; 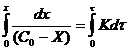
![]()
![]()
Все превращения радиоактивных веществ протекают по первому порядку. Уравнениями первого порядка описываются некоторые другие физические процессы, например, самопроизвольное излучение электронов невозбужденных атомов и молекул. По первому порядку протекает реакция ацетона:
![]()
Смотрите также
Получение, свойства и применение амидо-аммониевой соли малеопимаровой кислоты на основе малеинизированной канифоли
Республика Беларусь
располагает обширной сырьевой базой для развития лесохимической промышленности.
Одним из видов такого сырья является канифоль, которую получают из живицы путем
отгонки с ...


