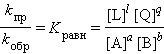Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Обратимые реакцииОткрытая химия / Химическая кинетика / Открытая химия / Химическая кинетика / Обратимые реакции Обратимые реакции
Особенность обратимых реакций состоит в том, что по мере накопления продуктов реакции возрастает скорость обратной реакции. Если они сравняются, то наступает равновесное состояние. Для реакции
| |
ЗДМ для прямой реакции Vпр = kпр [A]a [B]b, для обратной реакции Vобр = kобр [L]l [Q]q. При условии Vобр = Vпр получаем
| |
При отношении ![]() получаем выражение ЗДМ для обратимой реакции
получаем выражение ЗДМ для обратимой реакции
|
Для одностадийной реакции
| |
где k1 – константа скорости прямой реакции, k–1 – константа скорости обратной реакции.
При наступлении равновесия k1 [A] = k–1 [B], следовательно ![]()
Предположим, что А может превратиться в B через промежуточную стадию образования C: ![]()
Возможен ли такой циклический процесс? Оказывается, такой циклический процесс запрещен в силу принципа детального равновесия (микроскопической обратимости), согласно которому для равновесного химического процесса всякая элементарная реакция должна идти со скоростью, в точности равной скорости реакции. То есть, в обратимой элементарной реакции прямая и обратная реакции протекают через одно и то же переходное состояние. Справедлива схема ![]()
Эти шесть констант скорости не являются независимыми, поскольку k–1 k2 k3 = k1 k–2 k–3.
Смотрите также
Физико-химические свойства нефти, газа, воды и их смесей
...
Технология производства полиакрилонитрила
Полимер нитрила акриловой кислоты
(полиакрилонитрил) был впервые получен Моро в 1893 г. из этиленциангидрина и амида акриловой кислоты. Затем в 1931 г. Карозерс разработал метод пол ...
Гетерогенный катализ
Гомогенно-каталитизируемое
превращение протекает в одной фазе, где смешаны и реагенты, и катализатор, и
продукты. В гетерогенно-катализируемом превращении катализа-тор образует
отдельную фа ...