Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Определение массовой доли веществаУчим химию / Учим химию / Определение массовой доли вещества Определение массовой доли веществаСтраница 5
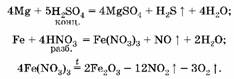
2. Вычислим количество вещества магния:
![]()
3. Вычислим количество вещества железа: 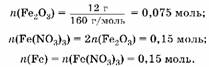
4. Определим соотношение металлов в смеси:!(Fe): Ti(Mg) ж 0,15: 0,3 ж 1: 2. Ответ: ra(Fe): ra(Mg) ж 1: 2.
Задача 10. Навеску смеси порошкообразных хрома и марганца обработали хлором без нагревания, масса навески при этом увеличилась на 2,13 г. Полученную смесь растворили в воде. Нерастворившийся твердый остаток отделили и обработали при нагревании концентрированной серной кислотой. Выделившийся газ был поглощен 60 мл 0,2 M раствора перманганата калия. Вычислите массу исходной навески.
Решение
1. С хлором без нагревания взаимодействует только марганец, при этом образуется соль MnCl2, растворимая в воде. С концентрированной серной кислотой при нагревании взаимодействует хром, причем образуется сульфат хрома(Ш) и выделяется SO2, который и взаимодействует с перманганатом калия:
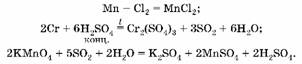
2. Найдем массу марганца:
![]()
то(Мп) ж 0,03 моль ■ 55 г/моль ж 1,65 г.
3. Найдем массу хрома:
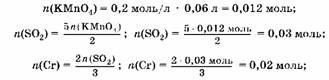
TO(Cr) ж 0,02 моль ■ 52 г/моль ж 1,04 г.
4. Вычислим массу исходной смеси:
то(см.) ж TO(Cr) K то(Мп); то(см.) ж 1,04 г K 1,65 г ж 2,69 г. Ответ: то(см.) ж 2,69 г.
Задача 11. При прокаливании смеси, содержащей равные количества вещества гидроксида, карбоната и нитрата двухвалентного металла, масса смеси уменьшилась на 25,5 г. Определите металл, входящий в состав соединений, а также массу смеси, если смесь не содержит примесей, а массовая доля металла в ней равна 46,83%.
Решение
1. Обозначим молярную массу металла через а количество вещества каждого компонента смеси — через Так как металл двухвалентен, а количества веществ в смеси равны, то масса металла равна 3,- (г).
Выразим массу исходной смеси:
то(исх. см.) ж то(Me(OH)2) K то(Me(NO3)2) K Tre(MeCO3); то(исх. см.) ж -(, K 34) K -(, K 124) K -(, K 60); то(исх. см.) ж 3,- K 218-.
2. Определим металл:
![]()
Решая это уравнение, получаем, ж 64, следовательно, металл — медь.
3. Напишем уравнения реакций:
(1) (2 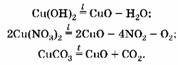 (3
(3
4. Найдем массу исходной смеси.
Так как масса смеси уменьшилась за счет образования газообразных продуктов реакции, то:
о(исх. см.) ж о(кон. см.) K 25,5;
то(исх. см.) ж - ■ 98 K - ■ 188 K - ■ 124; то(исх. см.) ж 410-;
то(кон. см.) ж TO1(CuO) K To2(CuO) K To3(CuO);
Следовательно, в смеси было по 0,15 моль веществ. Найдем ее массу:
то(исх. см.) ж 0,15 ■ 410 ж 61,5 (г). Ответ: Cu; то(исх. см.) ж 61,5 г.
Задача 12. Hитрат неизвестного металла растворили в воде и полученный раствор разделили на две равные части. К одной части добавили магний, к другой — такую же массу марганца. По окончании реакции масса осадка во второй части оказалась на 3,1 г меньше, чем в первой. После добавления избытка соляной кислоты к обоим осадкам они частично растворились, и их массы оказались равными и составили 21,6 г. Oπределите неизвестный металл.


