Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Коррозия железа
Оборудование и реактивы: 5 стаканов на 50 мл, 5 лабораторных пробирок, 5 железных гвоздей, вода дистиллированная, раствор хлорида натрия, раствор гидроксида натрия, медная и цинковая проволока.
Ход работы: Поместить железный гвоздь в пробирку, наполнить ее доверху водой и опрокинуть в стакан с водой. Таким же образом заготовить другие пробирки с гвоздями, но в место чистой воды в пробирки и в сосуды, в которые они будут опрокинуты, налить раствор хлорида натрия. В одном случае к этому раствору добавить немного раствора гидроксида натрия. К одному гвоздю заранее прикрепить медную проволоку, к другому - полоску или проволоку цинка. Примерно через сутки наблюдать процесс коррозии железного гвоздя и цинковой полоски. Объяснить наблюдаемые явления. Сравнить результаты опытов. Написать уравнения реакций.
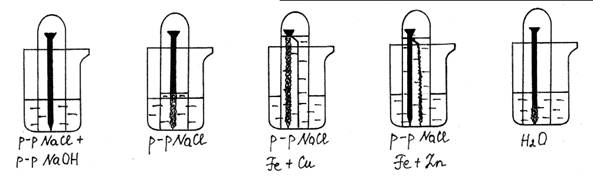
Рис. 31. Электрохимическая коррозия железа.
Утилизация. Все растворы из стаканов сливают в раковину, кроме раствора с соединениями цинка, который помещают в нейтрализатор.
Смотрите также
Прочносвязанные полисахариды в клеточных стенках ксиланового типа
Клеточная
стенка – один их немногих клеточных компартментов, наличие которого
принципиально отличает растительную клетку от животной. Казалось бы, она должна
пользоваться особым вниманием б ...


