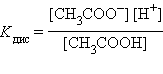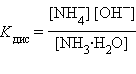Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Константы диссоциации кислот и
основанийОткрытая химия / Химическая термодинамика / Открытая химия / Химическая термодинамика / Константы диссоциации кислот и
оснований Константы диссоциации кислот и
оснований
Для слабых электролитов, к каковым относятся некоторые кислоты и основания, константа равновесия реакции диссоциации получила название константы диссоциации.
|
Реакция |
Константа диссоциации |
|
|
|
|
|
|
Поскольку эти константы – очень малые величины ![]() = 1,86∙10–5,
= 1,86∙10–5, ![]() = 1,77∙10–5), их выражают через отрицательный десятичный логарифм: – lg Kдисс = pKдисс. Тогда pK приведенных выше констант составят pKк = 4,730 и pKосн = 4,752.
= 1,77∙10–5), их выражают через отрицательный десятичный логарифм: – lg Kдисс = pKдисс. Тогда pK приведенных выше констант составят pKк = 4,730 и pKосн = 4,752.
Многоосновные кислоты и многокислотные основания характеризуются соответствующим числом ступенчатых констант диссоциации:
| |
|
| |
|
| |
|
| |
|
| |
|
Смотрите также
Количественный анализ силибина в экстрактах, полученных с использованием субкритической воды
Хорошее здоровье
– основа долгой, счастливой и полноценной жизни. Чтобы поддерживать здоровье,
необходимы знания о свойствах применяемых лекарств, лекарственных растений, а
также биологичес ...
Физические основы ограничения притока вод
Показаны факторы
преждевременного обводнения продуктивных пластов и скважин при заводнении
многопластовых нефтяных месторождений. Рассмотрены методы ограничения движения
воды в пористой сре ...
Получение медноаммиачного волокна (целлюлозы) химическим методом
Среди
различных видов искусственного волокна, которые изготовляются из целлюлозы,
медноаммиачное волокно занимает особое место. Этот вид искусственного волокна
впервые был по лучен давно: е ...