Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Энергия ГиббсаОткрытая химия / Химическая термодинамика / Открытая химия / Химическая термодинамика / Энергия Гиббса Энергия ГиббсаСтраница 2
Зависимость ΔH от температуры выражается соотношением ΔHT = ΔH° + ΔCp · ΔT, где ΔCp – изменение теплоемкости системы. Если в интервале температур 298 К – T реагенты не претерпевают фазовых превращений, то ΔCp = 0, и для расчетов можно пользоваться значениями ΔH°. информация здесь
Энтропия индивидуальных веществ всегда больше нуля и составляет от десятков до сотен Дж∙моль–1K–1 (табл. 4.1). Знак ΔG определяет направление реального процесса. Однако для оценки осуществимости процесса обычно пользуются значениями стандартной энергии Гиббса ΔG°. Величина ΔG° не может использоваться в качестве критерия вероятности в эндотермических процессах со значительным возрастанием энтропии (фазовые переходы, реакции термического разложнения с образованием газообразных веществ и др.). Такие процессы могут быть осуществлены за счет энтропийного фактора при условии
|
|
|
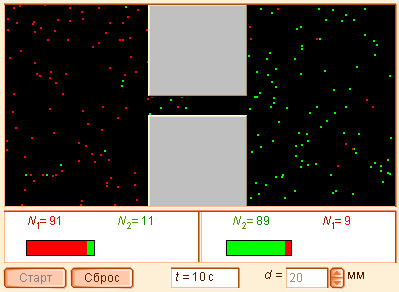
Модель 4.11. Диффузия газов |
Смотрите также
Фенолы. Реакции нуклеофильного замещения ароматических соединений. Получение фенолов
...
Роль химии в естествознании
...
Получение хлора методом электролиза повареной соли
Быстрое
развитие хлорной промышленности связано в основном с расширением производства
хлорорганических продуктов – винилхлоридов, хлорорганических растворителей,
инсектицидов и др. Хотя дол ...