Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Выбор стабильного сечения тройной
системы, продукты реакцийУчим химию / Участок по переработке лома твёрдых сплавов способом хлорирования / Учим химию / Участок по переработке лома твёрдых сплавов способом хлорирования / Выбор стабильного сечения тройной
системы, продукты реакций Выбор стабильного сечения тройной
системы, продукты реакцийСтраница 2
Кислород расходуется на образование WOCl4 и СО2 (см. стр. № 35 реакции 1 и 3), следовательно, необходимая масса кислорода равна:
![]() кг
кг
Хлор входит во все продукты реакций, и для изучения процесса хлорирования возмём хлор с избытком на 5%. Необходимая стехиометричеческая масса хлора равна:
![]()
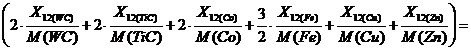
![]() кг
кг
Для моделирования процесса хлорирования твердого сплава возьмем данные из таблицы 4.2.1, 10000 кг хлора и 2443 кг кислорода.
Таблица 4.2.2.2. Результат моделирования процесса хлорирования при помощи прграммы TERRA, при температуре 700°C и давлении 0,1 МПа.
|
Химическая формула |
Масса [кг] |
|
WOCl4 |
12291,53 |
|
WO2Cl2 |
5,9 |
|
WCl4 |
0,3 |
|
WCl6 |
0,6 |
|
TiCl4 |
4239,3 |
|
CoCl2(c) |
1179,9 |
|
FeCl3 |
203,3 |
|
CuCl2(c) |
43,2 |
|
ZnCl2(c) |
28,4 |
|
ZnCl2 |
14,4 |
|
CO2 |
2567,6 |
|
Cl2 |
904,57 |
|
Всего: |
21479 |
4.2.2.1. Основные реакции протикающие при хлорировании твердосплавного лома
При рассмотрении таблицы 4.2.2.2 можно определить основные реакции.
1. ![]()
2. ![]()
3. ![]()
4. ![]()
5. ![]()
6. ![]()
4.2.2.2 Краткая характеристика продуктов реакций
Таблица 4.2.2.2.1. Краткая характеристика продуктов реакций [11].
|
Соединение |
Температура плавления [°С] |
Температура кипения [°С] |
Плотность [г/см3] |
|
WOCl4 – Оксодихлорид вольфкама (VI) |
212 |
~ 300 |
н. д. |
|
TiCl4 – Хлорид титана (IV) |
-24,1 |
+136,4 |
2,33(20°С) |
|
CoCl2 – Хлорид кобальта (II) |
740 |
1049 |
3,367 |
|
FeCl3 – Хлорид железа (III) |
307,5 |
316 |
2,898 |
|
CuCl2 – Хлорид меди (II) |
596 |
993 |
3,386 |
|
ZnCl2 – Хлорид цинка (II) |
293 |
733 |
2,907 |
Смотрите также
Адсорбция
Адсорбция (от лат. ad — на, при и sorbeo — поглощаю), поглощение к.-л. вещества
из газообразной среды или раствора поверхностным слоем жидкости или твёрдого
тела. Например, если поместить в ...
Пластические массы
Термин
"пластические массы" появился в конце XIX в. Первые промышленные материалы
были изготовлены на основе нитроцеллюлозы (1862-65) и казеина (1897). Развитие
современных реакто ...


