Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Определение конечной точки титрования.Библиотека / РН-метрия / Основы метода потенциометрического
титрования. / Библиотека / РН-метрия / Основы метода потенциометрического
титрования. / Определение конечной точки титрования. Определение конечной точки титрования.
Для определения конечной точки потенциометрического титрования можно использовать различные способы. Наиболее простой состоит в построении графика зависимости потенциала или рН от объема реагента (рис. 2.1. а). Затем визуально определяют среднюю точку участка, соответствующего вертикальному подъему кривой, и принимают ее за конечную точку. Предложены различные механические способы установления средней точки, но они ненамного улучшают точность ее нахождения.
Второй способ состоит в расчете изменения потенциала на единицу изменения объема реагента (т. е. нахождение ΔЕ/ΔV). График, построенный с использованием этого параметра как функции относительно объема, имеет острый максимум в конечной точке (рис. 2.1. б). С другой стороны, это отношение можно вычислить во время титрования и записать вместо потенциала. Как следует из данных, максимум находится между 24,3 и 24,4 мл; выбор 24,35 мл будет пригоден для большинства случаев.
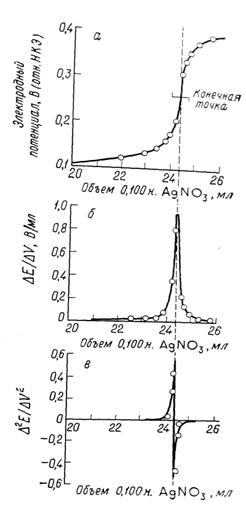
Рис. 2.1. Кривая потенциометрического титрования.
а) титрование 2,433 мэкв СІ- 0,1 н рас твором AgCI; б) кривая по первой производной; в) кривая по второй производной.
Лингейн [6] показал, что объем реагента можно зафиксировать более точно, определив точку, в которой вторая производная потенциала по объему (т. е. Δ2Е/ΔV2) равна нулю. Эти вычисления несложны, если вблизи точки эквивалентности добавляют равные порции раствора реагента.
Эта функция должна обратиться в нуль в некоторой точке между двумя объемами, где происходит перемена знака. Соответствующий этой точке объем получают интерполированием. Кривая в на рис. 2.1 представляет собой график зависимости Δ2Е/ΔV2.
Рассмотренные выше способы основаны на предположении, что кривая титрования симметрична относительно точки эквивалентности и перегиб кривой соответствует этой точке. Это допущение совершенно справедливо при условии, что вещества, участвующие в химической реакции, взаимодействуют друг с другом в эквимолярных соотношениях и что электродный процесс полностью обратим. Если эти условия не выполняются, получается асимметричная кривая титрования. Отметим, что кривая титрования железа (II) раствором церия (IV) симметрична относительно точки эквивалентности. С другой стороны, каждый моль перманганата окисляет пять молей железа (II), что приводит к получению совершенно асимметричной кривой титрования. Обычно вблизи точки эквивалентности этих кривых изменения потенциала достаточно велики, и поэтому если за конечную точку принять среднюю точку круто восходящего участка кривой титрования, то ошибка титрования будет незначительна. Только в том случае, если требуется чрезвычайно высокая точность или, если работают с очень разбавленными растворами, следует учитывать этот источник ошибок. При необходимости можно ввести эмпирическую поправку, проведя титрование стандартного раствора. С другой стороны, когда ошибка обусловлена несимметричностью реакции, точное положение точки эквивалентности можно рассчитать теоретически [6].
Другие способы обнаружения конечной точки включают титрование до теоретически рассчитанного значения потенциала электрода или, лучше, до потенциала, эмпирически установленного при титровании стандартных растворов.
Смотрите также
Теория строения, многообразие, классификация и номенклатура
органических соединений. Типы химических реакций
Многообразие органических соединений, их свойств
и превращений объясняет теория химического строения (А. М. Бутлеров,
1861–1864).
Химическое строение – это определенная последовательность располо ...
Железо
В периодической системе
железо находится в четвертом периоде, в побочной подгруппе VIII группы.
Химический знак – Fe (феррум). Порядковый
номер – 26, электронная формула 1s2 2s2 2p6
3d6 ...
Электролиз.
Цель работы - ознакомление
с процессами, протекающими на растворимых и нерастворимых электродах при
электролизе водных растворов электролитов.
Электролиз - это
окислительно-восстановительный ...


