Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Специфический кислотный или основной катализОрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Специфический кислотный или основной катализ Специфический кислотный или основной катализ
Между атомами электроотрицательных элементов (O, N и др.) перенос протона происходит очень быстро (см. разд. 2.3.2, гл. 2); поэтому во многих реакциях вначале устанавливается равновесие между реагентом R и его сопряженной кислотой RH+, а затем RH+ в лимитирующей скорость стадии образует продукт P. В случае водных растворов
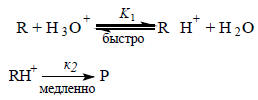
Применяя принцип стационарности, получаем
скорость = К1к2[R][H3O+].
Такая кинетика характерна, например, для гидролиза эфиров карбоновых кислот RCOOR в кислой среде. Протон, захваченный на первой стадии, возвращается в среду на второй стадии, и, следовательно, концентрация [H3O+] в ходе реакции остается постоянной. По этой причине [H3O+] можно исключить из выражения для скорости, и тогда получится уравнение реакции псевдопервого порядка, в которое не входит концентрация катализатора [H3O+]:
скорость = К1к2[R]
Тем не менее катализ легко обнаружить, если изучать кинетику при разных рН; тогда мы найдем, что константа скорости реакции псевдопервого порядка увеличивается пропорционально увеличению [H3O+] (рис. 3.9).
Если скорость реакции пропорциональна только концентрации [H3O+] (т.е. обратно пропорциональна рН), то такой случай называется специфическим кислотным катализом. В неводных средах специфический кислотный катализ осуществляется молекулами протонированного растворителя, например, NH4+ в жидком аммиаке, СН3СООН2+ в уксусной кислоте, H3SO4+ в 100%-ной H2SO4 и т.д. Кислота, сопряженная нейтральной молекуле растворителя, называется ионом лиония; следовательно, специфический кислотный катализ - это катализ ионами лиония.
Аналогично, если скорость реакции пропорциональна только концентрации гидроксильных ионов [OH-] (т.е. рН), то это означает, что наблюдается специфический основной катализ. С точки зрения механизма реакция, специфический основной катализ означает, что реакция начинается с быстрого отрыва протона от реагента гидроксильным ионом:
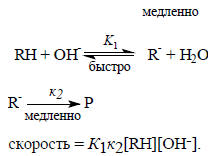
Примером такой реакции является альдольная конденсация:
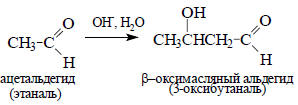
Основание, сопряженное нейтральной молекуле протонного растворителя, называется лиатным ионом; следовательно, специфический основной катализ - это катализ лиатным ионом (например, СН3О- в СН3ОН, димсиланионом CH3SOCH2- в ДМСО и т.д.).
Смотрите также
Определение карбонильных и карбоксильных групп в целлюлозе
Природная
целлюлоза характеризуется незначительным содержанием карбонильных групп.
Кетонные и карбоксильные группы в ней практически отсутствуют. При получении
технической целлюлозы из раст ...
Тяжелые металлы
Диагноз массового отравления жителей Рима
свинцом поставлен учеными спустя две тысячи лет. Раскопки показали, что древние
римляне пользовались водопроводной системой и посудой из свинца. Сви ...


