Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Применение принципа ЖМКООрганическая химия / Кислоты и основания / Органическая химия / Кислоты и основания / Применение принципа ЖМКО Применение принципа ЖМКО
Органические реакции. Проиллюстрируем, каким образом данные табл. 3.1 можно использовать для предсказания положения равновесия. Метанол и метилиодид формально можно представить как продукты нейтрализации мягкой кислоты СН3+ основаниями ОН- (жесткое) и I- (мягкое). Тогда на основании принципа ЖМКО можно "предсказать", что в реакции метанола с иодоводородом равновесие должно быть сдвинуто вправо, так как при этом образуются связи, соответствующие взаимодействию "мягкий-мягкий" и "жесткий-жесткий".
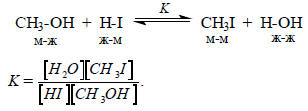
И действительно, константа равновесия очень велика: K≈109 при 25о С.
В другой приведенной ниже реакции происходит переход ацильного катиона (СН3С+=О, жесткая кислота) от мягкого основания RS- к жесткому основанию ОН-, и поэтому равновесие "должно" быть сдвинуто вправо:
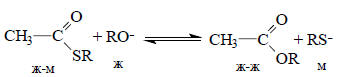
И действительно, эксперимент показывает, что тиоэфиры очень легко реагируют с водой и спиртами в слабощелочной среде.
Принцип ЖМКО широко применяется в органической химии, и мы будем его использовать в последующих главах этой книги. Например, этот принцип очень полезен при описании путей реакций амбидентных нуклеофилов, каковыми являются енолят-ионы, с электрофильными агентами (гл. 17):
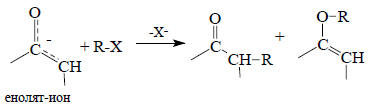
а также амбидентных электрофилов, например, α,β-ненасыщенных карбонильных соединений, с нуклеофилами (гл. 16):
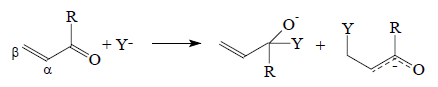
В первом случае в енолят-ионе углеродный нуклеофильный центр мягче, чем кислородный, и поэтому выход продукта алкилирования по углероду выше, если "кислотная часть" электрофила R-X (т.е. R+) является более мягкой кислотой Льюиса. Во второй реакции чем мягче нуклеофил Y-, тем выше его сродство к более мягкому электрофильному центру - β-углеродному атому, а не к более жесткому карбонилу. Поэтому для мягких нуклеофилов возрастает роль присоединения по β-атому С=С-связи (реакция Михаэля; см. гл. 16).
Симбиоз. На жесткость и мягкость донорного и акцепторного атомов в основаниях и кислотах соответственно оказывает влияние жесткость или мягкость заместителей, имеющихся в молекуле еще до образования аддукта. Этот эффект получил название "симбиоз". Суть его состоит в том, что мягкие заместители делают кислоты и основания более мягкими, жесткие заместители делают их более жесткими. Например, [Co(NH3)5F]2+ более стабилен, чем [Co(NH3)5I]2+, поскольку жесткое основание NH3 как бы увеличивает жесткость кобальта, делая его более склонным к присоединению фторида, а не иодида. С другой стороны, если аммиак заменить на мягкий лиганд CN-, то стабильность инвертируется: [Co(CN)5I]3- стабилен, а [Co(CN)5F]3- не существует.
Смотрите также
Физические и химические свойства диэлектриков
При выборе электроизоляционного
материала для конкретного применения приходится обращать внимание не только на
его электрические свойства в нормальных условиях, но рассматривать также их
с ...
Пирит
Пирит - минерал,
дисульфид железа FeS2, самый распространенный в земной коре сульфид.
Другие названия минерала и его разновидностей: кошачье золото, золото дурака,
железный колчедан, марказит, брав ...


