Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Взаимодействия "через связи"Органическая химия / Внутри- и межмолекулярные взаимодействия / Органическая химия / Внутри- и межмолекулярные взаимодействия / Взаимодействия "через связи" Взаимодействия "через связи"Страница 1
Как мы видели, разбор молекулы на "строительные кирпичи" позволяет легко строить ее МО в виде линейной комбинации орбиталей фрагментов. Вопрос о том, каким образом фрагментировать данную молекулу, решается тем, насколько легко далее получить картину взаимодействия орбиталей фрагментов. Данная пара орбиталей, направленная "через пространство" между фрагментами, комбинируется в фазе и в противофазе. Обычно комбинация в фазе имеет более низкую энергию, чем комбинация в противофазе. Однако в некоторых случаях комбинация в фазе может лежать выше по энергии, чем комбинация в противофазе.В качестве примера рассмотрим две неподеленные пары в молекуле 1,4-диазабицикло[2.2.2]октана, представляющего собой органический диамин. Прямое взаимодействие "через пространство" двух гибридных неподеленных пар приводит к образованию уровней n+ и n-, которые показаны ниже:
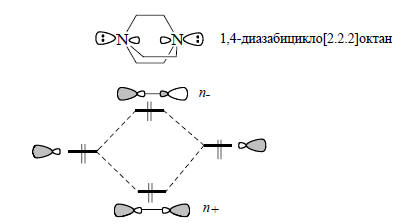
Вследствие того, что расстояние между атомами азота велико, энергетическое различие между n+ и n- должно быть небольшим. Тем не менее, расчеты и экспериментальные данные это не подтверждают. Так, две первые полосы в фотоэлектронных спектрах, которые обусловлены ионизацией уровней n+ и n-, отличаются между собой более чем не 2 эВ (7,52 и 9,65 эВ соответственно). Из анализа колебательных спектров диазабициклооктана следует, что уровень n+ лежит выше уровня n-. Такой порядок расположения уровней обусловлен тем фактом, что неподеленные электронные пары нельзя рассматривать изолированно от других частей молекулы. Эти пары взаимодействуют с σ и σ*-орбиталями связей С-С, находящихся между атомами азота (рис. 2.33). Такой эффект называется взаимодействие "через связь". Орбитали n+ и n- взаимодействуют с σ и σ*-орбиталями связей С-С. По сравнению с 1,4-взаимодействием неподеленных пар "через пространство" эти 1,2-взаимодействия (n+ с σ и n- с σ*) выражены гораздо сильнее. Под влиянием орбиталей σ и σ* энергия уровня n+ повышается, а энергия уровня n- - понижается. Это приводит к сильному расщеплению уровней, что и наблюдается в спектрах.
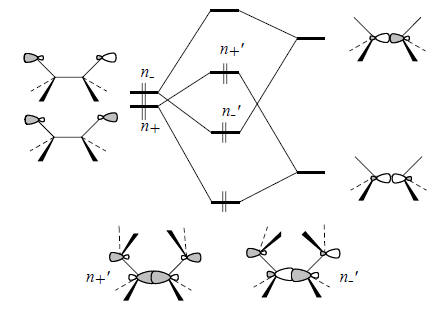 Рис. 2.33. Орбитальные взаимодействия "через связь" в молекуле 1,4-диазабицикло[2.2.2]октана
Рис. 2.33. Орбитальные взаимодействия "через связь" в молекуле 1,4-диазабицикло[2.2.2]октана
Аналогичная ситуация наблюдается в молекуле пиразина, в которой комбинация n+ лежит на 1,72 эВ выше по энергии, чем комбинация n- :
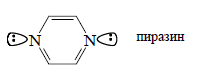
Конкуренция между взаимодействием "через пространство" и "через связи" часто дает очень интересные результаты. В качестве примера рассмотрим трицикло-3,7-октадиен, который может существовать или в анти-, или в син-конфигурации:
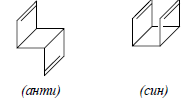
В анти-структуре взаимодействием π-орбиталей двойных связей "через пространство" можно пренебречь, но, по данным фотоэлектронной спектроскопии, различие между первым и вторым потенциалами ионизации для анти-формы (ΔIP=0,97 эВ) больше, чем для син-формы (ΔIP=0,36 ). Отсюда следует, что в анти-изомере двойные связи, далеко удаленные друг от друга, взаимодействуют между собой лучше, чем в син-изомере, где они находятся
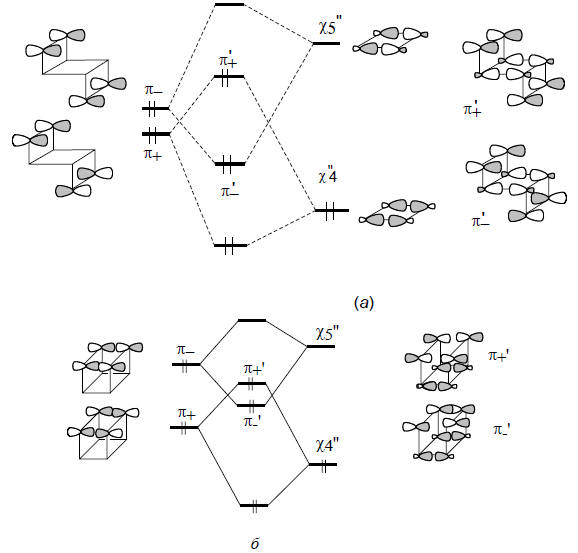 Рис. 2.34. Диаграмма взаимодействия в анти- (а) и син-изомерах (б) трицикло-3,7-октадиена
Рис. 2.34. Диаграмма взаимодействия в анти- (а) и син-изомерах (б) трицикло-3,7-октадиена
рядом. Этот парадокс объясняется взаимодействием "через связи". Как показано на рис. 2.34,а, взаимодействие "через пространство" в транс-изомере очень мало, и уровень π+ лежит лишь немного ниже уровня π-. С уровнями π+ и π- по симметрии могут взаимодействовать орбитали χ4"(χ3") и χ5"(χ6") соответственно. Вследствие взаимодействия "через связи" (π+ -χ4") и (π- -χ5") уровни π+ и π- меняются местами и сильно расходятся. В цис-изомере взаимодействие "через пространство" выражено гораздо сильнее, и расщепление уровней π+ и π- гораздо больше (рис. 2.34,б), причем, как и для транс-изомера, уровень π+ лежит ниже уровня π- . При взаимодействии "через связи" эти уровни меняются местами. Величина этого эффекта определяется 1,2-взаимодействями двойной связи с циклобутановым кольцом и для цис- и транс- изомеров примерно одинакова. Следовательно, повышение уровня π+ и понижение уровня π- в случае цис-изомера должно привести к меньшей величине энергетической щели между π+ и π-, что и наблюдается. Иными словами, большее взаимодействие "через пространство" в цис-изомере приводит к меньшей величине ΔIP из-за того, что проявляется противоположно направленный эффект.Во взаимодействиях "через связи" может участвовать не только одна -связь, но и две, три, четыре и т.д. σ-связей. С удлинением углеродной цепочки это взаимодействие не затухает, поскольку, по существу, оно является суммой последовательных 1,2-взаимодействий между соседними атомами. С другой стороны, взаимодействие "через пространство" сильно зависит от расстояния между взаимодействующими фрагментами и для длинных негибких цепей стремится к нулю. Ниже приведены примеры взаимодействия через две или три σ-связи:
Смотрите также
Нестероидные противовоспалительные препараты. Салицилаты
...
Определение карбонильных и карбоксильных групп в целлюлозе
Природная
целлюлоза характеризуется незначительным содержанием карбонильных групп.
Кетонные и карбоксильные группы в ней практически отсутствуют. При получении
технической целлюлозы из раст ...
Введение.
Уравнение
Ван-дер-Ваальса используется при исследовании процессов разделения и является
базовым уравнением при качественном исследовании этих процессов.
Распространение уравнения такого типа на мно ...


