Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
π-Системы, содержащие гетероатомОрганическая химия / Внутри- и межмолекулярные взаимодействия / Органическая химия / Внутри- и межмолекулярные взаимодействия / π-Системы, содержащие гетероатом π-Системы, содержащие гетероатомСтраница 1
Энергия возмущения выражается в единицах β и отсчитывается от стандартного уровня αС, который соответствует одиночной углеродной 2р-орбитали (поэтому индекс С) и называется несвязывающим уровнем. Однако, если мы переходим от чисто углеродных π-систем к системам, содержащим гетероатом, например, от этилена СН2=СН2 к формальдегиду СН2=О, от аллильного аниона СН2=СН-СН2- - к енолят-аниону ацетальдегида СН2=СН-О- или от бутадиена СН2=СН-СН=СН2 - к акролеину СН2=СН-СН=О, то кроме αС появляется второй уровень - αО, который соответствует одиночной 2р-орбитали атома кислорода. Поскольку αС ≠αО (уровень αО лежит ниже, так как кислород более электроотрицательный элемент, чем углерод), при образовании π-орбитали карбонильной группы >С=О происходит возмущение второго порядка (рис. 2.13).При возмущении второго порядка связывающая орбиталь напоминает более низко расположенную базисную невозмущенную орбиталь (см. разд. 2.5.3). Это выражается в коэффициентах и распределении электронной плотности. В этилене коэффциенты на обоих атомах углерода одинаковы (1/2, рис. 2.5), но в формальдегиде Cc<Co, a Cс*>Co*, причем Cc/Co= Cс*/ Co*. Это эквивалентно утверждению, что пара электронов на связывающей орбитали π «смещена» к атому кислорода, и на кислороде π- электронный заряд отрицательнее, а на углероде положительнее, чем в нейтральной молекуле этилена: Н2С=СН2, Н2Сδ+=Oδ− этилен формальдегид С другой стороны, плотность антисвязывающей орбитали π* больше на атоме углерода, чем на атоме кислорода.
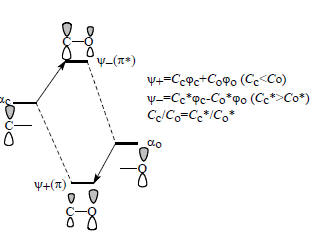 Рис. 2.13. Возмущение второго порядка при образовании π-связи карбонильной группы. Между ψ+ и ψ- находятся несвязывающие орбитали неподеленных пар электронов атома кислорода.
Рис. 2.13. Возмущение второго порядка при образовании π-связи карбонильной группы. Между ψ+ и ψ- находятся несвязывающие орбитали неподеленных пар электронов атома кислорода.
Необходимо иметь в виду, что орбиталь π не является высшей занятой МО карбонильной группы. У атома кислорода имеются две неподеленные пары электронов, которые занимают несвязывающие орбитали (почти вырожденные). Именно эти орбитали и будут ВЗМО. Локализация их на кислороде увеличивает общий отрицательный заряд на этом атоме. Реакции с электрофилами (например, с Н+) идут с участием как раз этих насвязывающих МО:
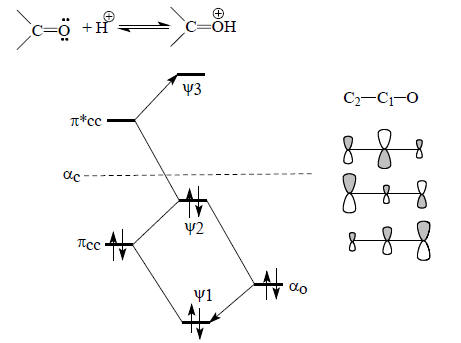 Рис. 2.14. π-Орбитали енолят-аниона ацетальдегида.
Рис. 2.14. π-Орбитали енолят-аниона ацетальдегида.
π-Система енолят-аниона (рис. 2.14) родственна аллильной π-системе (см. рис. 2.6). Связывающая π-орбиталь ψ1 в основном принадлежит атому кислорода в полной аналогии с соответствующей орбиталью карбонильной группы (рис. 2.13); она расположена очень низко, поскольку оба возмущения, как со стороны орбитали πСС этиленового фрагмента, так и со стороны орбитали π*СС, понижают уровень О2р. Орбиталь πСС расположена ближе к О2р, чем орбиталь π*СС, и поэтому взаимодействует с О2р сильнее, чем π*СС. Это можно выразить следующей схемой:
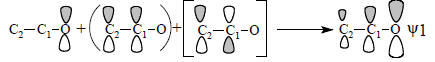
Смысл схемы состоит в том, что орбиталь ψ1 образуется из орбитали О2р путем смешивания ее с орбиталями πСС и π*СС в фазе (знак «плюс»). Орбиталь ψ1 по форме и по энергии похожа в первую очередь на О2р, во вторую очередь - на πСС и имеет лишь слабое сходство с π*СС. Действительно, π*СС имеет узел между С1 и С2, а ψ1 такого узла не имеет. Влияние π*СС на форму орбитали ψ1 угадывается лишь в том, что коэффициент при С2 меньше, чем при С1, так как π*СС подмешивается к πСС в области атома С2 в противофазе, а в области атома С1 - в фазе соответствующих р-функций.Орбитали ψ2 и ψ3 образуются следующим образом:
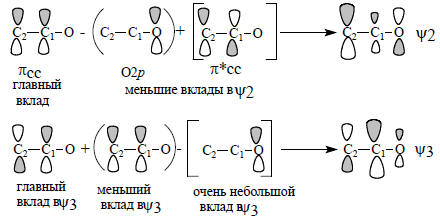
Орбиталь ψ2 расположена ниже уровня αС, но выше уровня αО. Поэтому между С1 и С2 имеется связывание, а между С1 и О - антисвязывание. Орбиталь ψ2 нельзя рассматривать в полном смысле как несвязывающую (в отличие от ψ2 аллила), так как коэффициент центрального атома С1 не равен нулю, но тем не менее коэффициент при очень мал (рис. 2.14), и поэтому реакции электрофилов по атому С1 маловероятны. И действительно, все реакции амбидентных анионов с электрофильными агентами идут или по О, или по С2 (гл. 17). Важным обстоятельством является тот факт, что в орбиталь ψ2 главный вклад вносит атом углерода С2, а не атом кислорода. Если учесть, что орбитали неподеленных пар электронов атома кислорода лежат ниже ψ2 (так как αО ниже ψ2; см. рис. 2.14), то можно прийти к заключению, что в реакциях с электрофилами, в которых важен орбитальный контроль, будет происходить атака по С2, а в реакциях с зарядовым контролем - атака по О (см. разд. 2.3.7), поскольку на атоме кислорода отрицательный заряд больше, чем не атоме углерода, из-за того что он имеет неподеленные пары, и, кроме того, нижняя занятая орбиталь ψ1 в основном принадлежит кислороду и лишь слабо делокализована по атомам углерода (см. рис. 2.14) Пустая орбиталь енолят-иона ψ3 локализуется в основном на С1, поэтому по С1 могла бы идти атака нуклеофилами. Однако енолят-анионы не склонны реагировать с нуклеофилами из-за того, что сами имеют отрицательный заряд, т.е. сами являются сильными нуклеофилами.Теперь обратим внимание на то, каковы коэффициенты, с которыми атомы О, С1 и С2 входят в данную орбиталь и в разные орбитали. При качественном рассмотрении будем называть эти коэффициенты «большой», «средний» и «небольшой» в соответствии с размерами р-АО на рис. 2.14. Можно составить следующую таблицу (табл. 2.7).
Смотрите также
Поверхностное натяжение и адсорбция на границе вода-воздух
...
Химические преобразователи солнечной энергии
Современная энергетика
опирается главным образом на такие источники, в которых запасена солнечная
энергия (СЭ). Прежде всего это ископаемые виды топлива, для образования которых
требуются ...


