Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Граничные орбиталиОрганическая химия / Внутри- и межмолекулярные взаимодействия / Органическая химия / Внутри- и межмолекулярные взаимодействия / Граничные орбитали Граничные орбитали
Когда реагируют между собой достаточно сложные молекулы Д и А, каждая из которых имеет и пустые, и заполненные орбитали, в принципе нужно рассматривать все взаимодействия как между занятыми орбиталями молекулы Д и вакантными орбиталями молекулы А, так и между вакантными орбиталями молекулы Д и занятыми орбиталями молекулы А. Единственным требованием является соответствие орбиталей по симметрии; если симметрия противоположная (когда относительно некоторой общей операции симметрии одна из орбиталей симметрична, а вторая антисимметрична), то энергия их взаимодействия равна нулю.Например, пусть молекула D имеет пять МО, три из которых заняты парами электронов, а молекула А - четыре МО: две занятые и две свободные, и пусть эти орбитали расположены так, как показано на рис. 2.4,а. Если учесть симметрию орбиталей (S - симметричная, А - антисимметричная) и не учитывать взаимодействия между двумя пустыми АО, то в этой системе возможно 8 парных взаимодействий между пустой и занятой орбиталями или между двумя занятыми орбиталями (рис. 2.4, б). Взаимодействия между занятыми и вакантными орбиталями стабилизируют комплекс DA, т.е. способствуют реакции D с А, однако энергия стабилизации для разных пар орбиталей различна, так как зависит от разности энергии взаимодействующих орбиталей ΔEα (уравнение (2.8)). Эта разность наименьшая для пары ψ3D/ψ3A (рис. 2.4, а). Именно на это наиболее сильное взаимодействие и следует в первую очередь обращать внимание при анализе реакционной способности молекул, хотя и другие взаимодействия могут вносить существенный вклад в реакции. Орбитали, между которыми происходит наиболее сильно выраженное взаимодействие, называются граничными орбиталями.
Граничные орбитали - это высшая занятая молекулярная орбиталь (ВЗМО) донора (молекулы D) и нижняя свободная молекулярная орбиталь (НСМО) акцептора (молекулы А; рис. 2.4). Молекула D характеризуется относительно высокой энергией ВЗМОD, а молекула А - относительно низкой энергией НСМОА; эти орбитали расположены ближе друг к другу, чем орбитали ВЗМОА и НСМОD (рис. 2.4, а). По этой причине можно утверждать, что в реакции D+A молекула D будет донором, а молекула А - акцептором электронов, но не наоборот. Донор (нуклеофил, основание Льюиса) характеризуется относительно высоким уровнем ВЗМО, а акцептор (электрофил, кислота Льюиса) - относительно низким уровне НСМО.
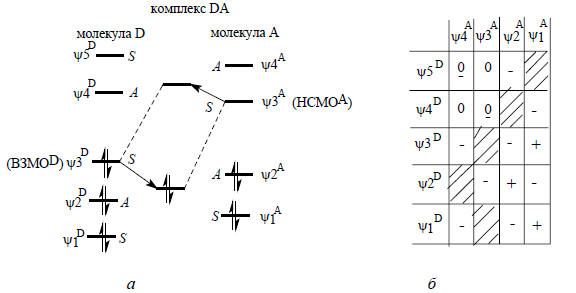 Рис. 2.4, а - Наиболее сильно взаимодействующие орбитали молекул D и А; б - возможные взаимодействия между орбиталями молекул D и А. Знак «+» означает дестабилизирующее взаимодействие между заполненными орбиталями. Заштрихованные клетки соответствуют стабилизирующему взаимодействию вакантных и заполненных орбиталей. Знаком «-» отмечены взаимодействия, запрещенные по симметрии, знаком «0» - взаимодействие двух пустых орбиталей.
Рис. 2.4, а - Наиболее сильно взаимодействующие орбитали молекул D и А; б - возможные взаимодействия между орбиталями молекул D и А. Знак «+» означает дестабилизирующее взаимодействие между заполненными орбиталями. Заштрихованные клетки соответствуют стабилизирующему взаимодействию вакантных и заполненных орбиталей. Знаком «-» отмечены взаимодействия, запрещенные по симметрии, знаком «0» - взаимодействие двух пустых орбиталей.
С учетом электростатического взаимодействия возмущение (Р), возникающее при контакте молекул D и А, можно выразить уравнением Р = 2(Cd Ca β)2/ΔEГМО - qdqa/r, (2.9) где ΔEГМО - разность уровней граничных молекулярных орбиталей. В этом уравнении первый член отражает понижение энергии вследствие орбитального взаимодействия, а второй член - также понижение энергии (так как обычно донорный атом d имеет частичный отрицательный заряд, и акцепторный атом а- частичный положительный заряд), но уже вследствие взаимодействия зарядов, т.е. электростатического притяжения.В некоторых реакциях главное влияние оказывает орбитальное взаимодействие, тогда говорят, что реакция имеет орбитальный контроль. Если преобладающее влияние оказывает электростатический член, то реакция имеет зарядовый контроль.Зарядовым и орбитальным контролем объясняется разный тип взаимодействия между жесткими и мягкими кислотами и основаниями. Эта важная концепция рассматривается в главе 3.
Смотрите также
Высокомолекулярные соединения и поверхностно активные вещества
...
Дериватографический анализ пирита
5-секундная активация
пирита приводит к заметному увеличению площади экзотермы, уменьшению
температурного интервала окисления и большей потере массы при нагревании.
Увеличение времени обработки в п ...


