Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Гомоядерные двухатомные молекулыОрганическая химия / Атомные и молекулярные орбитали / Органическая химия / Атомные и молекулярные орбитали / Гомоядерные двухатомные молекулы Гомоядерные двухатомные молекулыСтраница 3
В самом деле, зададим вопрос: какая из двух имеющихся 2рπ*-орбиталей (см. рис. 1.10) занята электронной парой? Оказывается, что по энергетическим соображениям гораздо лучшим размещением является 2рxπ*2рyπ*, а не 2рxπ*2, так как в первом случае электроны дальше отстоят друг от друга и поэтому меньше отталкиваются. Íî òîãäà ýëåêòðîíû çàíèìàþò ðàçíûå ïî ïðîñòðàíñòâåííîìó ïîëîæåíèю îðáèòàëè (орбитали 2рxπ* и 2рyπ* взаимно перпендикулярны, т.е. ортогональны), и принцип Паули уже не действует. Два электрона, расположенные по одному на ортогональных, имеют более низкую энергию, если их спины антипараллельны. Это общее правило, носящее название правила Хунда, предсказывает, что в молекуле О2 имеются два электрона с параллельными спинами. Отсюда следует, что молекула О2 имеет результирующий спиновый угловой момент, что обусловливает магнитный момент, т.е. молекула О2 должна быть магнитной. Это точно установлено экспериментально: жидкий кислород притягивается к магниту.
Имея два неспаренных электрона на разных орбиталях, кислород, таким образом, является бирадикалом. Поэтому часто для описания строения О2 используют формулу О.-О Однако использование этой формулы может привести к неправильному заключению, что один электрон принадлежит левому атому кислорода, а второй, с параллельным спином - правому атому. Лучше использовать изображенную ниже формулу, в которой линия, соединяющая атомы, изображает 2рσ-орбиталь, вертикальной квадратной скобкой изображается 2рxπ*-орбиталь, а горизонтальной - 2рyπ*-орбиталь. Для сравнения рядом приведена такая же формула для молекулы азота:
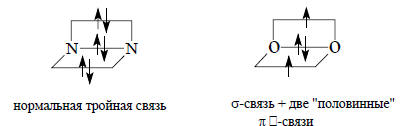
Приближенно можно считать, что в молекуле кислорода имеются три связи между атомами: нормальная двухэлектронная σ-связь и две слабые одноэлектронные π-связи.
Смотрите также
Получение хлора методом электролиза повареной соли
Быстрое
развитие хлорной промышленности связано в основном с расширением производства
хлорорганических продуктов – винилхлоридов, хлорорганических растворителей,
инсектицидов и др. Хотя дол ...
Замораживание как один из способов очистки питьевой воды от примесей
Вода, как природный
ресурс, является объектом государственной собственности во всех странах мира, в
которых первоочередное внимание уделяется вопросам управления, планирования и
экономики в ...
Определение уроновых кислот и полиуронидов
В состав кислых полисахаридов и полиуронидов древесины
входят звенья двух гексуроновых кислот — D-глюкуроновой
и D-галактуроновой. Звенья D-глюкуроновой
кислоты преимущественно содержатся в ...


