Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Связывающие и разрыхляющие орбиталиОрганическая химия / Атомные и молекулярные орбитали / Органическая химия / Атомные и молекулярные орбитали / Связывающие и разрыхляющие орбитали Связывающие и разрыхляющие орбиталиСтраница 2
Если взаимодействуют две атомные орбитали, то из них получаются две новые молекулярные орбитали: нижняя, связывающая МО, образуется путем перекрывания АО в фазе, а верхняя, антисвязывающая МО, - путем перекрывания АО в противофазе. Таким образом, антисвязывающая МО имеет на один узел больше чем связывающая, т.е. ее энергия выше.
В дальнейшем мы будем использовать упрощенные схемы образования молекулярных орбиталей из атомных орбиталей. Для иона Н2+. такая схема выглядит следующим образом:
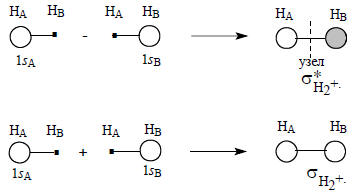
Знак «плюс» означает линейную комбинацию АО 1sA и 1sB в фазе, а знак «минус» - в противофазе. Подобные упрощенные схемы хорошо передают симметрию и узловые свойства МО, и этого часто бывает достаточно для анализа реакционной способности молекул. Тем не менее, эти схемы не показывают, насколько изменяются размеры АО при образовании МО, т.е. насколько электроны «поджимаются» к ядрам при образовании химической связи.
Смотрите также
Монокристаллический кремень
Основной объем
монокристаллического кремния (80-90%) потребляемого электронной
промышленностью, выращивается по методу Чохральского.
Фактически весь кремний,
используемый для производст ...
Белки и аминокислоты
Белки – это биологические полимеры, состоящие из аминокислот. Ни один из существующих живых организмов – от вирусов до растений и животных – не может существовать без белка. Правда, ...


