Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Нахождение молекулярной формулы органического соединенияCправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Cправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Нахождение молекулярной формулы органического соединения Нахождение молекулярной формулы органического соединенияСтраница 1
При выведении формул веществ, особенно в органической химии, часто используют относительную плотность газа.
Относительная плотность газа X – отношение абсолютной плотности этого (неизвестного) газа к абсолютной плотности другого (известного) газа В при одинаковых условиях:
![]()
Для 1 моль газа его абсолютная плотность равна
![]()
откуда
![]()
Если газ В задан, то
– плотность газа X по водороду
Н2 (М = 2 г/моль)
![]()
– плотность газа X по воздуху
(М = 29 г/моль)
![]()
и аналогично для любого другого известного газа X.
Примеры решения задач
1. В результате сгорания кислородсодержащего органического соединения в избытке воздуха собрано 1,584 г СO2 и O,972 мл Н2O. Плотность пара этого соединения по воздуху равна 1,5865.
Выведите формулу соединения, если в его молекуле содержатся два одноименных радикала.
Элементы ответа.
1) Составлена схема реакции:
![]()
2) Определена масса С и Н в этом соединении:
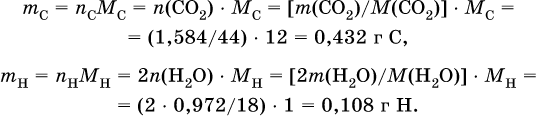
3) Определена формула соединения CxНyOz:
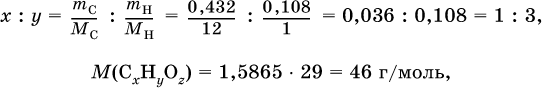
при х = 1 и у = 3: М(СН3) = 15, 46–15 = 31 г/моль на кислород – это не подходит,
при х = 2 и у = 6: 2М(СН3) = 30, М0 = 16, 30 + 16 = = 46 г/моль – это подходит, таким образом, искомая формула соединения С2Н6O, или с учетом условия (СН3)2O.
2. Некоторая масса неизвестного алкина с избытком хлора дает 21 г тетрахлор‑производного. Такая же масса того же алкина с избытком брома – 38,8 г тетрабром‑производного. Выведите формулу взятого алкина.
Элементы ответа.
1) Составлены уравнения реакций:
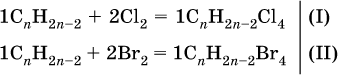
2) Составлены выражения для молярных масс производных:
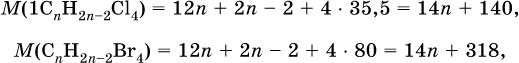
и для молярной массы алкина:
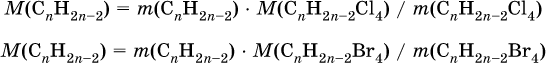
3) Выведена формула алкина: по условию масса алкина одинакова в реакциях (I) и (II), следовательно
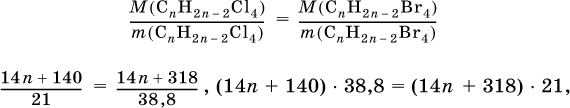
откуда n = 5 и формула алкина С5Н8.
Задания для самостоятельного решения части С
1. При сжигании углеводорода (плотность по воздуху равна 2) в кислороде образовалось 90 г воды. Выведите формулу углеводорода.
2. Гомолог этена массой 7 г присоединяет 2,24 л (н.у.) бромоводорода. Какова формула этого гомолога?
3. Выведите формулу некоторого углеводорода, если при сжигании в кислороде он образовал 6,6 г углекислого газа и 2,16 мл воды.
4. При полном сгорании некоторого арена в кислороде собрано 7,168 л (н.у.) углекислого газа. Выведите формулу этого углеводорода.
5. Выведите формулу одноатомного спирта, если при взаимодействии 27,6 г этого спирта с бромоводородом (в присутствии серной кислоты) получено 65,4 г бромалкана.
6. При сжигании 1,64 г органического соединения в избытке кислорода получено 1,06 г карбоната натрия, 1,12 л (н.у.) углекислого газа и 1,26 мл воды. Выведите формулу этого соединения.
7. Выведите формулу двухатомного спирта, при взаимодействии 9,3 г которого с кальцием собрано 3,36 л (н.у.) газа.
8. К 14 г смеси фенола и 0,05 моль гомолога бензола добавили бромную воду и получили 33,1 г осадка. Выведите формулу гомолога бензола.
Смотрите также
Кинетика химических реакций
Одна
из особенностей химических реакций заключается в том, что они протекают во
времени. Одни реакции протекают медленно, месяцами, как, например, коррозия
железа. Другие заканчиваются очень быстро ...
Фотоколориметрическое определение салициловой кислоты в фармпрепаратах
...


