Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Масса (объем, количество вещества) продукта по реагенту с
известной массовой долей в раствореCправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Cправочник по химии для подготовки к ЕГЭ / Решение расчетных задач / Масса (объем, количество вещества) продукта по реагенту с
известной массовой долей в растворе Масса (объем, количество вещества) продукта по реагенту с
известной массовой долей в растворе
Пример решения задачи
Навеску алюминия массой 13,7 г полностью сожгли в хлоре, а из образовавшейся соли приготовили 250 мл раствора. Пробу в 50 мл этого раствора слили с 68,4 мл 10,4 %‑ного раствора аммиака (плотность раствора 0,956 г/мл). Определите массу (в граммах) выпавшего осадка.
Элементы ответа.
1) Составлены уравнения реакций:
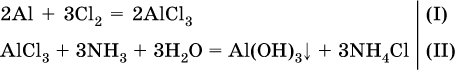
2) Определены количества AlCl3 в реакциях (I) и (II):
в реакции (I)
![]()
в реакции (II) взята 1/5 часть AlCl3, т. к.
![]()
отсюда
![]()
3) Определено количество NH3 в растворе для реакции (II):
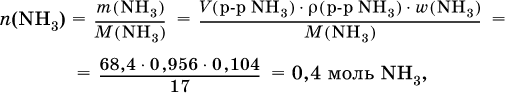
следовательно, NH3 – в избытке, и расчет далее ведется по AlCl3.
4) Определена масса Al(ОН)3 по уравнению (II): 0,1014 моль AlCl3 – 0,1014 моль Al(ОН)3,
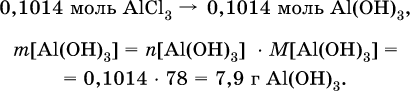
Задания для самостоятельного решения частей В, С
1. Приготовили раствор 134,4 л (н.у.) диоксида серы и добавили 1,5 л 25 %‑ного раствора гидроксида натрия (плотность раствора 1,28 г/мл). Определите массу (в граммах) образовавшейся соли.
2. Сульфид свинца (II) массой 95,6 г обрабатывают с помощью 300 мл 30 %‑ного раствора пероксида водорода (плотность раствора 1122,2 г/л). Рассчитайте массу (в граммах) продукта – сульфата свинца (II).
3. Смешали 100 г 5,64 %‑ного раствора фенола и 100 г 17,92 %‑ного раствора гидроксида калия. Найдите массовую долю (в %) избытка одного из реагентов в конечном растворе.
4. Установите массу (в граммах) железной пластинки после выдерживания в 110 мл 10 %‑го раствора CuSO4 (плотность раствора 1,1 г/мл), если до опыта ее масса составляла 11,5 г.
5. Вычислите объем (в литрах) 96 %‑ного водного спирта с плотностью 0,81 кг/л, полученного каталитической гидратацией 112 м3 (н.у.) этилена, содержащего 12,5 % (по объему) этана.
6. Газ, полученный сжиганием 44,8 л (н.у.) сероводорода в кислороде, поглощен с помощью 0,5 л 25 %‑ного раствора гидроксида натрия (плотность раствора 1,275 г/ мл). Определите массовую долю (в %) соли в конечном растворе.
7. Углекислый газ объемом 15 л (н.у.) пропущен через 560 г 5%‑ного раствора гидроксида калия. Найдите массу (в граммах) соли, полученной в этом процессе.
8. Железная пластинка массой 5 г опущена на некоторое время в 50 мл 15 %‑ного раствора сульфата меди (II) с плотностью 1,12 г/мл. Масса пластинки увеличилась на 0,16 г. Какова массовая доля (в %) сульфата меди (II) в оставшемся растворе?
9. По реакции Кучерова получен этаналь, который переведен в соответствующую кислоту в виде 100 г 6%‑ного водного раствора. Найдите объем (в литрах, н.у.) исходного органического соединения в получении этаналя.
10. Определите массовую долю (в %) избытка одного из реагентов в растворе после сливания 80 г 10 %‑ного раствора гидроксида натрия и 2O г 18,25 %‑ной хлороводородной кислоты.
11. Установите объем (в литрах, н.у.) газа, собранного после внесения 0,3 моль алюминия в 160 мл 20 %‑ного раствора гидроксида калия (плотность раствора 1,19 г/мл).
12. Найдите массу (в граммах) органического продукта, полученного при смешивании 250 г 94 % – ного водного раствора фенола и 2143 г 3,5 %‑ной бромной воды.


