Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ФосфорCправочник по химии для подготовки к ЕГЭ / Неметаллы главных подгрупп IV–VII групп / Cправочник по химии для подготовки к ЕГЭ / Неметаллы главных подгрупп IV–VII групп / Фосфор ФосфорСтраница 1
Фосфор – элемент 3‑го периода и VA‑группы Периодической системы, порядковый номер 15. Электронная формула атома [10Ne]3s23p3, устойчивая степень окисления в соединениях +V.
Шкала степеней окисления фосфора:
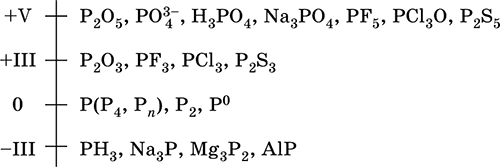
Электроотрицательность фосфора (2,32) значительно ниже, чем у типичных неметаллов, и немного выше, чем у водорода. Образует различные кислородсодержащие кислоты, соли и бинарные соединения, проявляет неметаллические (кислотные) свойства. Большинство фосфатов нерастворимы в воде.
В природе – тринадцатый
по химической распространенности элемент (шестой среди неметаллов), встречается только в химически связанном виде. Жизненно важный элемент.
Недостаток фосфора в почве восполняется введением фосфорных удобрений – главным образом суперфосфатов.
Красный и белый фосфор Р.
Известно несколько аллотропных форм фосфора в свободном виде, главные – это белый фосфор Р4 и красный фосфор Рn. В уравнениях реакций аллотропные формы представляют как Р (красн.) и Р (бел.).
Красный фосфор состоит из полимерных молекул Рn разной длины. Аморфный, при комнатной температуре медленно переходит в белый фосфор. При нагревании до 416 °C возгоняется (при охлаждении пара конденсируется белый фосфор). Нерастворим в органических растворителях. Химическая активность ниже, чем у белого фосфора. На воздухе загорается только при нагревании.
Применяется как реагент (более безопасный, чем белый фосфор) в неорганическом синтезе, наполнитель ламп накаливания, компонент намазки коробка при изготовлении спичек. Не ядовит.
Белый фосфор состоит из молекул Р4. Мягкий как воск (режется ножом). Плавится и кипит без разложения (tпл 44,14 °C, tкип 287,3 °C, ρ 1,82 г/см3). Окисляется на воздухе (зеленое свечение в темноте), при большой массе возможно самовоспламенение. В особых условиях переводится в красный фосфор. Хорошо растворим в бензоле, эфирах, сероуглероде. Не реагирует с водой, хранится под слоем воды. Чрезвычайно химически активен. Проявляет окислительно‑восстановительные свойства. Восстанавливает благородные металлы из растворов их солей.
Применяется в производстве Н3РO4 и красного фосфора, как реагент в органических синтезах, раскислитель сплавов, зажигательное средство. Горящий фосфор следует гасить песком (но не водой!). Чрезвычайно ядовит.
Уравнения важнейших реакций:

Получение в промышленности– восстановление фосфорита раскаленным коксом (песок добавляют для связывания кальция):
Са3(РO4)2 + 5С + 3SiO2 = 3CaSiO3 + 2Р
+ 5СО (1000 °C)
Пар фосфора охлаждают и получают твердый белый фосфор.
Красный фосфор готовят из белого фосфора (см. выше), в зависимости от условий степень полимеризации n (Рn) может быть различной.
Фосфин РН3.
Бинарное соединение, степень окисления фосфора равна – III. Бесцветный газ с неприятным запахом. Молекула имеет строение незавершенного тетраэдра [: Р(Н)3] (sр3‑гибридизация). Мало растворим в воде, не реагирует с ней (в отличие от NH3). Сильный восстановитель, сгорает на воздухе, окисляется в HNO3 (конц.). Присоединяет HI. Применяется для синтеза фосфорорганических соединений. Сильно ядовит.
Уравнения важнейших реакций:
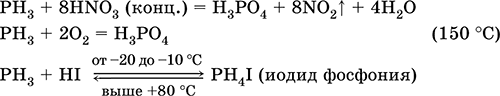
Получение в лаборатории
:
Са3Р2 + 6НCl (разб.) = ЗСаCl2 + 2РН3
↑
Оксид фосфора (V) Р2O5.
Кислотный оксид. Белый, термически устойчивый. В твердом и газообразном состояниях димер Р4О10 со строением из четырех тетраэдров [O=Р(O)3], связанных по трем вершинам (Р – О–Р). При очень высоких температурах мономеризуется до Р2O5. Существует также стеклообразный полимер (Р2O5)n. Чрезвычайно гигроскопичен, энергично реагирует с водой, щелочами. Восстанавливается белым фосфором. Отнимает воду у кислородсодержащих кислот.
Применяется как весьма эффективный дегидратирующий агент для осушения твердых веществ, жидкостей и газовых смесей, реагент в производстве фосфатных стекол, катализатор полимеризации алкенов. Ядовит.
Уравнения важнейших реакций:
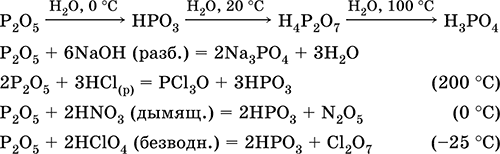
Получение: сжигание фосфора (см.) в избытке сухого воздуха.
Ортофосфорная кислота Н3РO4.
Смотрите также
Модифицированные эпоксидные композиции пониженной горючести
...
Производство аммиака: краткая характеристика
Общей экономической
задачей каждого химического предприятия является получение химических веществ высокого
качества и в достаточном количестве, чтобы их реализация приносила прибыль. С этим
...


