Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
ВодородCправочник по химии для подготовки к ЕГЭ / Неметаллы главных подгрупп IV–VII групп / Cправочник по химии для подготовки к ЕГЭ / Неметаллы главных подгрупп IV–VII групп / Водород ВодородСтраница 2
Применяется водород как восстановитель и гидрирующий агент в синтезе технически важных продуктов (редкие металлы, NH3, НCl, органические вещества).
Вода Н2O.
Бинарное соединение. Бесцветная жидкость (слой более 5 м толщиной окрашен в голубой цвет), без вкуса и запаха. Молекула имеет строение дважды незавершенного тетраэдра [:: ОН2] (sр3‑гибридизация). Летучее вещество, термически устойчивое до 1000 °C.
В обычных условиях полярные молекулы воды образуют между собой водородные связи. Это обусловливает аномалию температур плавления и кипения воды – они значительно выше, чем у ее химических аналогов (H2S и других). Затвердевание воды в лед сопровождается увеличением объема на 9 %, т. е. лед легче жидкой воды (вторая аномалия воды). Наибольшую плотность вода имеет не при 0 °C, а при 4 °C (третья аномалия воды). Твердая вода (лед) легко возгоняется.
Природная вода по изотопному составу водорода в основном 1Н2O с примесью 1Н2НО и 2Н2O, по изотопному составу кислорода в основном Н216O с примесью Н218O и Н217O. В малой степени подвергается диссоциации до Н+, или, точнее, до Н3O+, и ОН; очень слабый электролит. Катион оксония Н3O+ имеет строение незавершенного тетраэдра [: O(Н)3] (sр3‑гибридизация). Образует кристаллогидраты со многими солями, аквакомплексы – с катионами металлов. Реагирует с металлами, неметаллами, оксидами. Вызывает электролитическую диссоциацию кислот, оснований и солей, гидролизует многие бинарные соединения и соли. Подвергается электролизу в присутствии сильных электролитов. Почти универсальный жидкий растворитель неорганических веществ.
Для химических целей природную воду очищают перегонкой (дистиллированная вода), для промышленных целей умягчают, устраняя «временную» и «постоянную» жесткость, или полностью обессоливают, пропуская через иониты в кислотной Н+‑форме и щелочной ОН‑ – форме (ионы солей осаждаются на ионитах, а ионы Н+ и ОН‑ переходят в воду и взаимно нейтрализуются). Питьевую воду обеззараживают хлорированием (старый способ) или озонированием (современный, но дорогой способ; озон не только окисляет вредные примеси подобно хлору, но и увеличивает содержание растворенного кислорода).
Уравнения важнейших реакций:
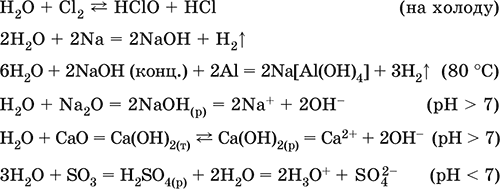
Примеры гидролиза бинарных соединений:
6H2O + Al2S3 = 2Al(ОН)3↓ + 3H2S↑
2H2O + SF4 = SO2↑ + 4HF↑ (40–60 °C)
6H2O + Mg3N2 = 3Mg(OH)2↓ + 2NH3↑ (кипячение)
2H2O + CaC2 = Ca(OH)2↓ + C2H2↑
Вода – окислитель за счет HI:
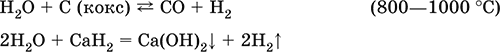
Электролиз воды:
![]()
Электропроводность чистой (дистиллированной) воды весьма мала, поэтому электролиз проводят в присутствии сильных электролитов.
а) в нейтральном
растворе (электролит Na2SO4)
катод 2H2O + 2е‑ = H2↑ + 2OH
анод 2Н2O – 4е‑ = O2↑ + 4H+
раствор ОН‑ + Н+ = Н2O
б) в кислом
растворе (электролит H2SO4)
катод 2Н+ + 2е‑ = Н2↑
анод 2Н2O – 4е‑ = O2↑ + 4Н+
в) в щелочном
растворе (электролит NaOH)
катод 2Н2O + 2е‑ = Н2↑ + 2OН‑
анод 4OН‑ – 4е‑ = O2↑ + 2Н2O
Один из методов обнаружения воды основан на переходе во влажной атмосфере белого сульфата меди(II) CuSO4 в голубой медный купорос CuSO4 5Н2O.
Известна изотопная разновидность воды – тяжелая вода D2O (2Н2O); в природных водах массовое отношение D2O: Н2O = 1: 6000.
Плотность, температуры плавления и кипения тяжелой воды выше, чем у обыкновенной. Растворимость большинства веществ в тяжелой воде значительно меньше, чем в обычной воде. Она ядовита, так как замедляет биологические процессы в живых организмах. Тяжелая вода накапливается в остатке электролита при многоразовом электролизе воды. Используется как теплоноситель и замедлитель нейтронов в ядерных реакторах.
Смотрите также
Получение серной кислоты путем переработки отходов производства диоксида титана
Сернокислотный
метод производства диоксида титана из ильменита и титановых шлаков имеет ряд
существенных недостатков — сложная многостадийная схема, высокий расход серной
кислоты, значитель ...


