Меню сайта
Наши новости
Распространение алкалоидов в растительном мире.
Умягчение воды
Жидкофазное и газофазное гидрирование углеводородовСтатьи и работы по химии / Статьи и работы по химии / Жидкофазное и газофазное гидрирование углеводородов Жидкофазное и газофазное гидрирование углеводородовСтраница 3
При прочих равных условиях селективность зависит от времени контакта, определяющего фактическую степень конверсии исходного вещества. Чем ближе она к равновесной, тем значительнее развитие последовательных реакций более глубокого гидрирования. Обычно гидрирование проводят до высокой (до 90%) степени конверсии. Но для каждого процесса время контакта определяется экспериментально.
Все реакции присоединения водорода являются экзотермическими и обратимыми. Теплота гидрирования алкенов с двойной связью на конце молекулы (пропилен, бутен-1) больше, чем алкенов с двойной связью, расположенной ближе к середине цепи (бутен-2).
При расчете на одну молекулу присоединяющегося водорода тепловой эффект наиболее высок для соединений со связью СºС.
СНºСН + 2Н2 ® СН3-СН3 (-DН = 311 кДж/моль)
Для ароматических систем он меньше, чем для олефинов, что может быть обусловлено нарушением устойчивости ароматической системы.
С6Н6 + 3Н2 ® С6Н12 (-DН = 206 кДж/моль)
RCH=CH2 + H2 ® RCH2-CH3 (-DН = 113-134 кДж/моль)
При гидрировании двойной связи между углеродом и кислородом в карбонильных соединениях тепловой эффект ниже, чем для двойной углерод - углеродной связи
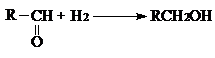
(-DН = 67-68 кДж/моль)
при этом гидрирование альдегидов более экзотермично, чем гидрирование кетонов:
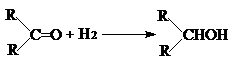
(-DН = 67-68 кДж/моль)
Близкий к ним тепловой эффект (в расчете на одну молекулу водорода) имеет гидрирование нитрилов:
RCN + 2H2 ® RCH2NH2 (-DН = 134-159 кДж/моль).
Наименьший тепловой эффект наблюдается при гидрировании кислот:
RCOOH + 2H2 ® RCH2OH + H2O (-DН = 38-42 кДж/моль)
и деструктивном гидрировании связи С-С
-СН2-СН2- + Н2 ® -СН3 + -СН3 (-DН = 42-63 кДж/моль)
Особенности оформления реакционного узла газофазного гидрирования углеводородов. Равновесие реакций гидрирования. Специфика применения катализаторов различного типа при проведении реакций гидрирования. Кинетика реакций гидрирования
.
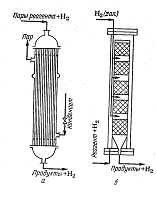
Реакционные аппараты для газофазного гидрирования:
а) трубчатый реактор; б) колонна со сплошными слоями гетерогенного катализатора и охлаждением холодным водородом
Реакция гидрирования обратима. Обратный процесс – дегидрирование. Вследствие экзотермичности реакций гидрирования равновесная степень превращения увеличивается при понижении температуры.
Термодинамически наиболее благоприятно протекает гидрирование ацетиленовых производных, наименее – гидрирование кислот.
Поскольку при гидрировании (за исключением деструктивного) всегда происходит уменьшение объема. Для увеличения равновесной степени превращения, особенно при высокой температуре, применяют повышенное давление. Другим методом повышения степени превращения является применение избытка водорода по сравнению со стехиометрическим от 5010-кратного до 100-кратного и более. Часто одновременно применяется и повышенное давление, и избыток водорода.
Смотрите также
Технология получения и свойства мочевино-формальдегидных смол
Первые
продукты конденсации мочевины с формальдегидом (карбамидные смолы) были
получены еще в 1896 г., но производство мочевино-альдегидных смол налажено лишь
в 1920—1921 гг.
Мочевино-фо ...
Особенности сорбционного извлечения палладия (II) из хлоридных растворов волокнами ЦМ-А2, Мтилон-Т и ВАГ
Одним из
перспективных направлений в комплексном решении экологических проблем является
разработка высокоэффективных процессов очистки промышленных газовоздушных
выбросов, сточных вод и сре ...
Расчёт многокорпусной выпарной установки
В химической промышленности выпариванию подвергают
растворы твердых веществ (главным образом водные растворы щелочей, солей и
др.), а также растворы высококипящих жидкостей, обладающих при т ...


